题目内容
【题目】某兴趣小组对NH4NO3的热分解产物提出如下4种猜想:
甲:N2、HNO3、H2O 乙:N2O、NO、H2O
丙:NH3、N2、H2O 丁:N2、NO、H2O
你认为猜想有科学性不正确的是( )
A.甲和乙B.乙和丁C.乙和丙D.丙和丁
【答案】C
【解析】
A、NH4NO3中N元素的化合价有-3和+5两种,原子个数比为1:1,根据得失电子守恒,若发生归中反应生成氮气,消耗-3价N和+5价N的比为5:3,所以+5价N有剩余,有硝酸生成,不可能有氨气生成,故甲有可能、丙不可能;若发生归中反应,![]() 、
、![]() ,根据得失电子守恒,-3价N和+5价N的比为3:4,所以-3价N有剩余,应有氨气生成,故乙不可能;若发生归中反应,
,根据得失电子守恒,-3价N和+5价N的比为3:4,所以-3价N有剩余,应有氨气生成,故乙不可能;若发生归中反应,![]() 、
、![]() ,根据得失电子守恒, 消耗-3价N和+5价N的比为1:1,可能不生成其他含N的产物,故丁有可能;故选C。
,根据得失电子守恒, 消耗-3价N和+5价N的比为1:1,可能不生成其他含N的产物,故丁有可能;故选C。

练习册系列答案
相关题目
【题目】等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示:
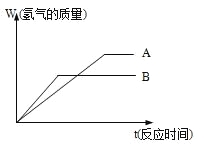
(1) 两种金属的活动性顺序是_____>______
两种金属氯化物的摩尔质量是_____>______
(2) 将两种金属粉末按一定比例混合后,进行甲、乙
丙三组实验,三组实验各取500mL同浓度的盐酸
溶液加入该种混合粉末,产生气体,有关数据如下:
实验序号 | 甲 | 乙 | 丙 |
混合粉末质量(g) | 6.2 | 18.6 | 24.8 |
生成气体气体(mL) | 2240 | 5600 | 5600 |
①乙组实验中,盐酸________(填“过量”、“适量”或“不足量”)
②上述所用的盐酸的物质的量浓度为_____mol/L,混合粉末的平均摩尔质量是________。