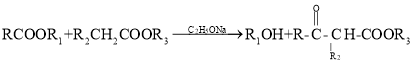
题目内容
【题目】根据物质结构有关性质和特点,回答下列问题:
(1)Ti基态原子核外电子排布式为____________,碳原子的价电子轨道表示式为________。
(2)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积____________(填“膨胀”或“收缩”)。
(3)写出一种与NH4+互为等电子体物质的化学式____________。
(4)SO2的空间构型为___________________。
(5)丙烯腈(CH2=CH—CN)分子中σ键和π键的个数比为____,分子中碳原子轨道杂化类型是______。
(6)FeCl3熔点282℃,而FeCl2熔点674℃,二者熔点差异的原因是______________。
【答案】[Ar]3d24s2 ![]() 膨胀 CH4或SiH4 V形 2:1 sp2、sp 氯化亚铁为离子晶体,熔化时需要破坏离子键;而氯化铁为分子晶体,熔化时需要破坏分子间作用
膨胀 CH4或SiH4 V形 2:1 sp2、sp 氯化亚铁为离子晶体,熔化时需要破坏离子键;而氯化铁为分子晶体,熔化时需要破坏分子间作用
【解析】
(1)Ti为22号元素,碳为6号元素,据此分析书写;
(2)六方最密堆积空间利用率大于体心立方堆积;
(3)与NH4+互为等电子体的微粒中需要含有5个原子、8个价电子;
(4)根据价层电子对个数=σ键个数+孤电子对个数计算判断;
(5)丙烯腈可以写成CH2=CH—C≡N,据此判断σ键和π键的数目;价层电子对个数是3的碳原子采用sp2杂化,价层电子对个数是2的C原子采用sp杂化,据此分析判断;
(6)根据晶体类型与熔沸点的关系分析解答。
(1)Ti原子3d能级上2个电子、4s能级上2个电子为其价电子,其电子排布式为[Ar]3d24s2;基态碳原子核外有6个电子,其中价电子为4,分布在2s、2p轨道上,价电子轨道表示式为![]() ,故答案为:[Ar]3d24s2;
,故答案为:[Ar]3d24s2; ![]() ;
;
(2)六方最密堆积空间利用率大于体心立方堆积,所以由α-Ti转变为β-Ti晶体体积膨胀,故答案为:膨胀;
(3)与NH4+互为等电子体的微粒中含有5个原子、8个价电子,与其互为等电子体的微粒有CH4、SiH4等,故答案为:CH4(或SiH4);
(4)SO2中S原子的价层电子对数=2+![]() =3,原子轨道空间构型为平面三角形,分子构型为V形,故答案为:V形;
=3,原子轨道空间构型为平面三角形,分子构型为V形,故答案为:V形;
(5)共价单键为σ键、共价双键中含有1个σ键、1个π键,共价三键中含有1个σ键、2个π键,则丙烯腈(CH2=CH—C≡N)分子中含有6个σ键、3个π键,所以σ键与π键个数之比=6∶3=2∶1;价层电子对个数是3的碳原子采用sp2杂化,价层电子对个数是2的C原子采用sp杂化,前两个碳原子价层电子对个数是3、后一个碳原子价层电子对个数是2,所以前两个碳原子采用sp2杂化,后一个采用sp杂化,故答案为:2∶1;sp2、sp;
(6)氯化亚铁为离子晶体,氯化铁为分子晶体,离子键的作用力大于分子间作用力,导致氯化亚铁的熔点比氯化铁的熔点高的多,故答案为:氯化亚铁为离子晶体,熔化时需要破坏离子键;而氯化铁为分子晶体,熔化时需要破坏分子间作用。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案【题目】二氧化碳资源化利用是目前研究的热点之一。
(1)二氧化碳可用于重整天然气制合成气(CO和H2)。
①已知下列热化学方程式:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206kJ/mol,CO2(g)+4H2(g)
CO(g)+3H2(g) △H1=+206kJ/mol,CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) △H 2=-165kJ/mol,
CH4(g)+2H2O(g) △H 2=-165kJ/mol,
则反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)的△H=____kJ/mol。
2CO(g)+2H2(g)的△H=____kJ/mol。
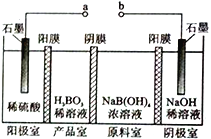
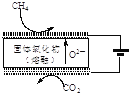
②最近我国学者采用电催化方法用CO2重整CH4制取合成气,装置如图所示。装置工作时,阳极的电极反应式为________。
(2)由二氧化碳合成VCB(锂电池电解质的添加剂)的实验流程如下,已知EC、VCB核磁共振氢谱均只有一组峰,均含五元环状结构,EC能水解生成乙二醇。
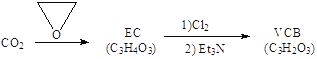
VCB的结构简式为_________。
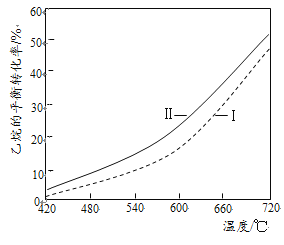
(3)乙烷直接热解脱氢和CO2氧化乙烷脱氢的相关化学方程式及平衡转化率与温度的关系如下:
(I)乙烷直接热解脱氢:C2H6(g)![]() C2H4(g)+H2(g) △H1
C2H4(g)+H2(g) △H1
(Ⅱ)CO2氧化乙烷脱氢:C2H6(g)+CO2(g)![]() C2H4(g)+CO(g)+H2O(g) △H2
C2H4(g)+CO(g)+H2O(g) △H2
①反应(I)的△H1= ____kJ/mol(填数值,相关键能数据如下表)。
化学键 | C-C | C=C | C-H | H-H |
键能/kJ·mol-1 | 347.7 | 615 | 413.4 | 436.0 |
②反应(Ⅱ)乙烷平衡转化率比反应(I)的大,其原因是______(从平衡移动角度说明)。
③有学者研究纳米Cr2O3催化CO2氧化乙烷脱氢,通过XPS测定催化剂表面仅存在Cr6+和Cr3+,从而说明催化反应历程为:C2H6(g)→C2H4(g)+H2(g),______和_______(用方程式表示,不必注明反应条件)。
④在三个容积相同的恒容密闭容器中,温度及起始时投料如下表所示,三个容器均只发生反应:C2H6(g)img src="http://thumb.zyjl.cn/questionBank/Upload/2019/10/07/08/dcc46cb6/SYS201910070801057716573811_ST/SYS201910070801057716573811_ST.001.png" width="33" height="10" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />C2H4(g)+H2(g)。温度及投料方式(如下表所示),测得反应的相关数据如下:
容器1 | 容器2 | 容器3 | |
反应温度T/K | 600 | 600 | 500 |
反应物投入量 | 1molC2H6 | 2molC2H4+2molH2 | 1molC2H6 |
平衡时v正(C2H4)/ mol/(L·s) | v1 | v2 | v3 |
平衡时c(C2H4)/ mol/L | c1 | c2 | c3 |
平衡常数K | K1 | K2 | K3 |
下列说法正确的是_______(填标号)。
A.K1=K2,v1<v2 B.K1<K3,v1< v3 C.v2>v3,c2>2c3 D.c2+c3<3c1
【题目】硫酰氯(SO2Cl2)和亚硫酰氯(SOCl2)常用作氯化剂,都可用于医药、农药、染料工业及有机合成工业。亚硫酰氯还用于制锂亚硫酰氯(Li/SOCl2)电池。
有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 ②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 具有吸水性且难分解 |
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的热化学方程式为:SO2(g)+Cl2(g) ![]() SO2Cl2(l) △H= - 97.3 kJ·mol-1。反应装置如图所示(夹持仪器已省略),请回答有关问题:
SO2Cl2(l) △H= - 97.3 kJ·mol-1。反应装置如图所示(夹持仪器已省略),请回答有关问题:

(1)仪器A的名称为___________;
(2)仪器B的作用是_____________________;
(3)装置丙中盛放的试剂为____________,在实验室用氢氧化钠吸收多余硫酰氯反应的离子方程式为___________________;
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有_________(填序号)
①先通冷凝水,再通气体 ②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温 ④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的实验操作名称为__________________,
②设计实验方案检验氯磺酸分解制取硫酰氯产品中混有硫酸,下列方案合理的是:_____(填字母)
A.取样品溶于水,滴加紫色石蕊溶液变红:再取少量溶液,加入BaCl2溶液产生白色沉淀,说明含有H2SO4。
B.取样品在干燥条件下加热至完全反应,冷却后直接加BaCl2溶液,有白色沉淀,再滴加紫色石蕊溶液变红,说明含有H2SO4。
(6)Li—SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2===4LiCl+S+SO2。
①写出该电池正极发生的电极反应式_______________________________
②组装该电池必须在无水、无氧的条件下进行,原因是__________________