题目内容
12.化学来源于生活,服务于生活,请你用学过的化学知识解决生活中的实际问题.(1)家庭用煤经过从“煤球”到“蜂窝煤”的变化,其原因是增大了煤与氧气的接触面积,能使煤充分燃烧
(2)据调查,煤燃烧时能排放出二氧化硫气体,易导致酸雨,请写出酸雨的危害腐蚀建筑物,毁坏庄稼,使土壤酸化,使水体显酸性等写出一条减少酸雨生成的合理化建议改用天然气或其它清洁能源等.
分析 (1)促进可燃物燃烧的方法有:增大可燃物与氧气的接触面积或增大氧气的浓度;
(2)酸雨能腐蚀建筑物,毁坏庄稼,使土壤酸化,使水体显酸性.
解答 解:(1)家庭用煤经过从“煤球”到“蜂窝煤”的变化,增大了煤与氧气的接触面积,能使煤充分燃烧,故答案为:增大了煤与氧气的接触面积,能使煤充分燃烧;
(2)酸雨的危害有:腐蚀建筑物,毁坏庄稼,使土壤酸化,使水体显酸性等;改用天然气或其它清洁能源等,故答案为:腐蚀建筑物,毁坏庄稼,使土壤酸化,使水体显酸性等;改用天然气或其它清洁能源等.
点评 本题化学反应速率与环境污染等,难度不大,掌握促进可燃物燃烧的方法(增大可燃物与氧气的接触面积或增大氧气的浓度)是正确解答本题的关键.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
3.下列物质所属的类别正确的是( )
| A. | 纯碱--盐 | B. | 干冰--混合物 | ||
| C. | 澄清石灰水--纯净物 | D. | 洁净的空气--纯净物 |
11.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是Ar(填元素符号)
(2)②③⑦三种元素的原子半径从大到小的顺序为Cl>N>O(填元素符号)
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式HClO4,碱性最强的化合物的名称氢氧化钾.
(4)元素⑤的氧化物与元素④的最高价氧化物对应水化物反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O.
(5)元素⑥和⑦形成的气态氢化物较稳定是HCl(填化学式),用方程式来说明元素⑦的非金属性比⑥的非金属强的事实Cl2+H2S=S↓+2HCl(一个或两个方程式均可)
(6)表示①与③形成的化合物的电子式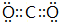 ,写出它的一种用途做灭火剂等.
,写出它的一种用途做灭火剂等.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | Ⅵ | VⅡA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)②③⑦三种元素的原子半径从大到小的顺序为Cl>N>O(填元素符号)
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式HClO4,碱性最强的化合物的名称氢氧化钾.
(4)元素⑤的氧化物与元素④的最高价氧化物对应水化物反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O.
(5)元素⑥和⑦形成的气态氢化物较稳定是HCl(填化学式),用方程式来说明元素⑦的非金属性比⑥的非金属强的事实Cl2+H2S=S↓+2HCl(一个或两个方程式均可)
(6)表示①与③形成的化合物的电子式
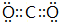 ,写出它的一种用途做灭火剂等.
,写出它的一种用途做灭火剂等.
8.下列反应必须加入氧化剂才能实现的是( )
| A. | CH4→CO2 | B. | KMnO4→K2MnO4 | C. | SO2→SO32- | D. | H2O2→O2 |
10.下列各项叙述中,正确的是( )
| A. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| B. | 24Cr原子的电子排布式是1s22s22p63s23p63d44s2 | |
| C. | 所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |

 如图,一密闭气缸被一不漏气可滑动的活塞隔成两部分,左室充有氮气,右室充有混合气体.在室温下将右室的气体点燃,反应后冷却至原室温,活塞最终静止于气缸的某一点(液体体积忽略不计).
如图,一密闭气缸被一不漏气可滑动的活塞隔成两部分,左室充有氮气,右室充有混合气体.在室温下将右室的气体点燃,反应后冷却至原室温,活塞最终静止于气缸的某一点(液体体积忽略不计).