题目内容
7.将11.1g CaCl2溶于水配成100mL溶液,此溶液的物质的量浓度为1mol/L,取此溶液10mlCa2+的浓度为1mol/L,含Cl-0.02NA个.分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=cV结合物质的构成计算.
解答 解:n(CaCl2)=$\frac{11.1g}{111g/mol}$=0.1mol,c(CaCl2)=$\frac{0.1mol}{0.1L}$=1mol/L,
取此溶液10mlCa2+的浓度为1mol/L,
N(Cl-)=1mol/L×2×0.01L×NA=0.02NA,
故答案为:1mol/L;1mol/L;0.02NA.
点评 本题考查物质的量的相关计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握物质的构成特点以及相关计算公式的运用,难度不大.

练习册系列答案
相关题目
19.实验室中需要配制2mol/L的NaOH溶液850mL,配制时应选用的容量瓶的规格和称取的NaOH的质量分别是( )
| A. | 950mL,76g | B. | 500mL,80g | C. | 1000mL,80g | D. | 1000mL,76g |
16.等物质的量的下列物质与足量稀硝酸反应,氧化产物伪Cu2-或SO42-还原产物为N0,消耗硝酸的量最多的是( )
| A. | Cu | B. | Cu2O | C. | CuS | D. | Cu2S |
3.下列各组物质中,互为同系物的是( )
| A. | CH3-CH=CH2和 | B. | 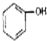 和 和 | C. |  和 和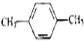 | D. | 乙酸和油酸 |