ΧβΡΩΡΎ»ί
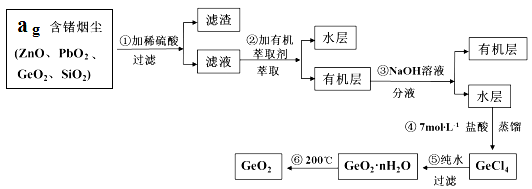
ΓΨΧβΡΩΓΩ”“ΆΦ «Η÷Χζ‘Ύ≥± ΣΩ’ΤχάοΖΔ…ζΒγΜ·―ßΗ· ¥ΒΡ Ψ“βΆΦΘ§ΖΔ…ζΒΡΖ¥”ΠΈΣΘΚ
2FeΘΪ2H2OΘΪO2ΘΫ2Fe(OH)2ΓΘFe(OH)2ΦΧ–χ±Μ―θΜ·ΈΣFe(OH)3Θ§Fe(OH)3Ά―Υ°…ζ≥…Χζ–βΓΘ«κΗυΨίΆΦ ΨΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ

Θ®1Θ©‘Ύ…œ ωΒγΜ·―ßΗ· ¥÷–Θ§ΧΦΘ®CΘ©Ής ΦΪΓΘ
Θ®2Θ©–¥≥ωΗΚΦΪΒΡΒγΦΪΖ¥”Π Ϋ ΓΘ
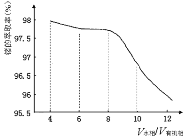
Θ®3Θ©ΙΛ“Β…œΘ§≥Θ‘ΎΗ÷Χζ…η±ΗΒΡ±μΟφΆΩ“Μ≤ψ”ΆΘ§ΤδΉς”Ο « ΓΘ
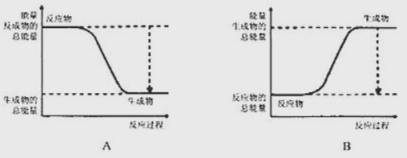
AΘ°Φθ…ΌΗ÷Χζ”κΩ’ΤχΚΆΥ°ΒΡΫ”¥ΞΘ§Ζά÷Ι‘ΎΗ÷Χζ±μΟφ–Έ≥…ΈΔ–Γ‘≠Βγ≥Ί
BΘ°ΗτΨχΗ÷Χζ”κΩ’ΤχΚΆΥ°ΒΡΫ”¥ΞΘ§Ήη÷Ι‘ΎΗ÷Χζ±μΟφ–Έ≥…ΈΔ–ΓΒγΫβ≥Ί
CΘ°»σΜ§…η±ΗΘ§Ζά÷ΙΜ“≥ΨΈέ»Ψ
DΘ°Ζά÷Ι»ΥΈΣΫ”¥Ξ…η±ΗΘ§±ήΟβ…η±ΗΗ· ¥
Θ®4Θ©»γΙϊΫΪ≥ΛΤΎΫΰ≈ί‘ΎΚ”Υ°÷–ΒΡΗ÷Χζ’ΔΟ≈”κΆβΒγ‘¥Ν§Ϋ”ΖάΗ·Θ§”ΠΫΪ’ΔΟ≈Ν§Ϋ”Άβ≤Ω÷±ΝςΒγ‘¥ΒΡ ΦΪΓΘ
ΓΨ¥πΑΗΓΩΘ®1Θ©’ΐΘ®2Θ©FeΘ≠2eΘ≠= Fe2+ Θ®3Θ©A Θ®4Θ©ΗΚ
ΓΨΫβΈωΓΩ
‘ΧβΖ÷ΈωΘΚΘ®1Θ©Χζ‘Ύ≥± ΣΩ’ΤχάοΖΔ…ζΒγΜ·―ßΗ· ¥Θ§ΧζΉςΗΚΦΪΘ§±ΜΗ· ¥Θ§CΉς’ΐΦΪΘΜ
Θ®2Θ©ΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣFeΘ≠2eΘ≠= Fe2+ ΘΜ
Θ®3Θ©ΙΛ“Β…œΘ§≥Θ‘ΎΗ÷Χζ…η±ΗΒΡ±μΟφΆΩ“Μ≤ψ”ΆΘ§ΤδΉς”Ο «Φθ…ΌΗ÷Χζ”κΩ’ΤχΚΆΥ°ΒΡΫ”¥ΞΘ§Ζά÷Ι‘ΎΗ÷Χζ±μΟφ–Έ≥…ΈΔ–Γ‘≠Βγ≥ΊΘΜ
Θ®4Θ©»γΙϊΫΪ≥ΛΤΎΫΰ≈ί‘ΎΚ”Υ°÷–ΒΡΗ÷Χζ’ΔΟ≈”κΆβΒγ‘¥Ν§Ϋ”ΖάΗ·Θ§”ΠΫΪ’ΔΟ≈Ν§Ϋ”Άβ≤Ω÷±ΝςΒγ‘¥ΒΡΗΚΦΪΘ§ΗΟΖΫΖ® «ΆβΫ”ΒγΝςΒΡ“θΦΪ±ΘΜΛΖ®ΓΘ

ΓΨΧβΡΩΓΩΒΣΒΡ«βΜ·ΈοNH3ΓΔN2H4Β»‘ΎΙΛ≈©“Β…ζ≤ζΓΔΚΫΩ’ΚΫΧλΒ»Νλ”ρ”–ΙψΖΚ”Π”ΟΓΘ
Θ®1Θ©“ΚΑ±ΉςΈΣ“Μ÷÷«±‘ΎΒΡ«εΫύΤϊ≥Β»ΦΝœ“―‘Ϋά¥‘Ϋ±Μ―–ΨΩ»Υ‘±÷Ί ”ΓΘΥϋ‘ΎΑ≤»Ϊ–‘ΓΔΦέΗώΒ»ΖΫΟφΫœΜ· ·»ΦΝœΚΆ«β»ΦΝœ”–Ή≈Ϋœ¥σΒΡ”≈ ΤΓΘΑ±ΒΡ»Φ…’ Β―ι…φΦΑœ¬Ν–ΝΫΗωœύΙΊΒΡΖ¥”ΠΘΚ
ΔΌ4NH3(g)ΘΪ5O2(g)ΘΫ4NO(g)ΘΪ6H2O(l) ΓςH1
ΔΎ4NH3(g)ΘΪ6NO(g)ΘΫ5N2(g)ΘΪ6H2O(l) ΓςH2
‘ρΖ¥”Π 4NH3(g)ΘΪ3O2(g)ΘΫ2N2(g)ΘΪ6H2O(l) ΓςHΘΫ ΓΘΘ®«κ”ΟΚ§”–ΓςH1ΓΔΓςH2ΒΡ ΫΉ”±μ ΨΘ©
Θ®2Θ©Κœ≥…Α± Β―ι÷–Θ§‘ΎΧεΜΐΈΣ3 LΒΡΚψ»ίΟή±’»ίΤς÷–Θ§ΆΕ»κ4 mol N2ΚΆ9 mol H2‘Ύ“ΜΕ®ΧθΦΰœ¬Κœ≥…Α±Θ§ΤΫΚβ ±ΫωΗΡ±δΈ¬Ε»≤βΒΟΒΡ ΐΨί»γœ¬±μΥυ ΨΘΚ
Έ¬Ε»(K) | ΤΫΚβ ±NH3ΒΡΈο÷ ΒΡΝΩ(mol) |
T1 | 2.4 |
T2 | 2.0 |
“―÷ΣΘΚΤΤΜΒ1 mol N2(g)ΚΆ3 mol H2(g)÷–ΒΡΜ·―ßΦϋœϊΚΡΒΡΉήΡήΝΩ–Γ”ΎΤΤΜΒ2 mol NH3(g)÷–ΒΡΜ·―ßΦϋœϊΚΡΒΡΡήΝΩΓΘ
ΔΌ‘ρT1 T2Θ®ΧνΓΑΘΨΓ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±Θ©ΓΘ
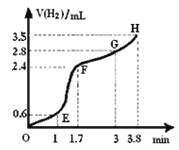
ΔΎ‘ΎT2 Kœ¬Θ§Ψ≠Ιΐ10min¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§Θ§‘ρ0~10minΡΎH2ΒΡΤΫΨυΥΌ¬ v(H2)= Θ§ΤΫΚβ ±N2ΒΡΉΣΜ·¬ ΠΝΘ®N2Θ©= ΓΘ
Δέœ¬Ν–ΆΦœώΖ÷±π¥ζ±μλ ±δΘ®ΓςHΘ©ΓΔΜλΚœΤχΧεΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩΘ®![]() Θ©ΓΔN2ΧεΜΐΖ÷ ΐΠ’Θ®N2Θ©ΚΆΤχΧεΟήΕ»Θ®Π―Θ©”κΖ¥”Π ±ΦδΒΡΙΊœΒΘ§Τδ÷–’ΐ»Ζ«“Ρή±μΟςΗΟΩ…ΡφΖ¥”Π¥οΒΫΤΫΚβΉ¥Χ§ΒΡ « ΓΘ
Θ©ΓΔN2ΧεΜΐΖ÷ ΐΠ’Θ®N2Θ©ΚΆΤχΧεΟήΕ»Θ®Π―Θ©”κΖ¥”Π ±ΦδΒΡΙΊœΒΘ§Τδ÷–’ΐ»Ζ«“Ρή±μΟςΗΟΩ…ΡφΖ¥”Π¥οΒΫΤΫΚβΉ¥Χ§ΒΡ « ΓΘ
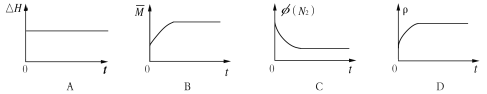
Θ®3Θ©Ρ≥N2H4Θ®κ¬ΜρΝΣΑ±Θ©»ΦΝœΒγ≥ΊΘ®≤ζ…ζΈ»Ε®ΓΔΈόΈέ»ΨΒΡΈο÷ Θ©‘≠άμ»γΆΦ1Υυ ΨΓΘ
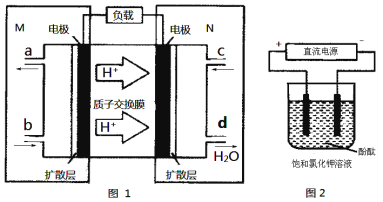
ΔΌM«χΖΔ…ζΒΡΒγΦΪΖ¥”Π ΫΈΣ ΓΘ
ΔΎ”Ο…œ ωΒγ≥ΊΉωΒγ‘¥Θ§”ΟΆΦ2ΉΑ÷ΟΒγΫβ±ΞΚΆ¬»Μ·ΦΊ»ή“ΚΘ®ΒγΦΪΨυΈΣΕη–‘ΒγΦΪΘ©Θ§…η±ΞΚΆ¬»Μ·ΦΊ»ή“ΚΧεΜΐΈΣ500mLΘ§Β±»ή“ΚΒΡpH÷Β±δΈΣ13 ±Θ®‘Ύ≥ΘΈ¬œ¬≤βΕ®Θ©Θ§»τΗΟ»ΦΝœΒγ≥ΊΒΡΡήΝΩάϊ”Ο¬ ΈΣ80%Θ§‘ρ–ηœϊΚΡN2H4ΒΡ÷ ΝΩΈΣ gΘ®ΦΌ…η»ή“ΚΒγΫβ«ΑΚσΧεΜΐ≤Μ±δΘ©ΓΘ