题目内容
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题:
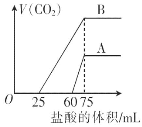
(1)原NaOH溶液的物质的量浓度为_______________。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是____________,其物质的量之比为___。
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况下)的最大值为____mL。
(4)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-889.6 kJ·mol-1①
N2(g)+2O2(g)===2NO2(g)ΔH=+67.7 kJ·mol-1②
则CH4还原NO2生成水蒸气和氮气的热化学方程式是_____________。
【答案】0.75mol/LNaOH与Na2CO33:1112mLCH4(g)+2NO2(g)= N2(g)+2H2O(g)+CO2(g) ΔH=-956.3 kJ·mol-1
【解析】
(1)加入75mL盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液。根据氯离子、钠离子守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.075mL×0.1mol/L=0.0075mol,
所以c(NaOH)=![]() =0.75mol/L;
=0.75mol/L;
(2)CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H2O,当n(CO2):n(NaOH)≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成生成NaHCO3,CO2有剩余;
当![]() <n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
<n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
当n(CO2):n(NaOH)≤![]() ,反应按②进行,等于
,反应按②进行,等于![]() ,时,CO2、NaOH恰好反应生成Na2CO3;小于
,时,CO2、NaOH恰好反应生成Na2CO3;小于![]() 时,生成Na2CO3,NaOH有剩余;
时,生成Na2CO3,NaOH有剩余;
由曲线A可知从60mL到75mL为碳酸氢钠与盐酸反应,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(NaHCO3)=n(HCl)=(0.075-0.06)L×0.1mol/L=1.5×10-3mol,根据C原子守恒,所以n(CO2)=n(NaHCO3)=1.5×10-3mol,由(1)可知,n(NaOH)=0.0075mol,所以n(CO2):n(NaOH)=1.5×10-3mol:0.0075mol=1:5,小于1:2,所以反应按②进行,NaOH有剩余,溶液中溶质为Na2CO3和NaOH。根据C原子守恒,所以n(Na2CO3)=n(CO2)=1.5×10-3mol,再根据钠离子守恒,得溶液中氢氧化钠的物质的量为0.0075mol-1.5×10-3mol×2=0.0045mol,所以溶液中NaOH与Na2CO3的物质的量之比为0.0045mol:1.5×10-3mol=3:1;
(3)由曲线B可知从25mL到75mL为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(CO2)=n(HCl)=(0.075ml-0.025ml)×0.1mol/L=0.005mol,所以CO2气体体积为0.005mol×22.4L/mol=0.112L=112mL;
(4)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH1=-889.6 kJ·mol-1;
②N2(g)+2O2(g)==2NO2(g) ΔH2=+67.7 kJ·mol-1;
根据盖斯定律,由①-②得反应:CH4(g)+2NO2(g)= N2(g)+2H2O(g)+CO2(g) ΔH=ΔH1-ΔH2=-889.6 kJ·mol-1-67.7 kJ·mol-1=-956.3 kJ·mol-1;则CH4还原NO2生成水蒸气和氮气的热化学方程式是CH4(g)+2NO2(g)= N2(g)+2H2O(g)+CO2(g) ΔH=-956.3 kJ·mol-1。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案