题目内容
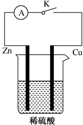 某同学为了探究原电池产生电流的过程,设计了如图所示实验.
某同学为了探究原电池产生电流的过程,设计了如图所示实验.(1)打开开关K,观察到锌片溶解,表面产生大量气泡,铜片表面无明显现象,写出有关反应的离子方程式
(2)关闭开关K,观察到电流表指针偏转,锌片溶解,铜片表面产生大量气泡.若在标准状况下,产生气体体积为3.36L,则转移电子的物质的量是
(3)关闭开关K,如果锌极和铜极都产生气泡,可能的原因是
如果使用纯锌,其他条件相同,打开K和关闭K产生气泡速率较快的是
考点:探究原电池及其工作原理
专题:电化学专题
分析:(1)打开开关K,观察到锌片溶解,表面产生大量气泡,铜片表面无明显现象,其反应实质是锌和酸发生置换反应;
(2)关闭开关K,观察到电流表指针偏转,锌片溶解,铜片表面产生大量气泡,说明该装置构成原电池,锌作负极、Cu作正极,正极上氢离子放电,根据氢气和转移电子之间的关系式计算;
(3)原电池能加快金属腐蚀.
(2)关闭开关K,观察到电流表指针偏转,锌片溶解,铜片表面产生大量气泡,说明该装置构成原电池,锌作负极、Cu作正极,正极上氢离子放电,根据氢气和转移电子之间的关系式计算;
(3)原电池能加快金属腐蚀.
解答:
解:(1)打开开关K,观察到锌片溶解,表面产生大量气泡,铜片表面无明显现象,说明锌和酸发生置换反应、铜不发生反应,离子方程式为Zn+2H+═=Zn2++H2↑,故答案为:Zn+2H+═=Zn2++H2↑;
(2)关闭开关K,观察到电流表指针偏转,锌片溶解,铜片表面产生大量气泡,说明该装置构成原电池,锌作负极、Cu作正极,正极上氢离子放电生成氢气,电极反应为2H++2e-=+H2↑,根据氢气和转移电子之间的关系得转移电子的物质的量=
×2=0.3mol,故答案为:0.3mol;
(3)关闭开关K,如果锌极和铜极都产生气泡,说明铜和锌、稀硫酸构成原电池,锌和锌中某些物质及稀硫酸构成原电池,所以锌中含有杂质;
原电池能加快负极金属的腐蚀速率,所以如果使用纯锌,其他条件相同,打开K和关闭K产生气泡速率较快的是关闭K时产生气泡较快,
故答案为:锌片不纯,含杂质的锌片在稀硫酸中构成原电池;关闭K时产生气泡较快.
(2)关闭开关K,观察到电流表指针偏转,锌片溶解,铜片表面产生大量气泡,说明该装置构成原电池,锌作负极、Cu作正极,正极上氢离子放电生成氢气,电极反应为2H++2e-=+H2↑,根据氢气和转移电子之间的关系得转移电子的物质的量=
| 3.36L |
| 22.4L/mol |
(3)关闭开关K,如果锌极和铜极都产生气泡,说明铜和锌、稀硫酸构成原电池,锌和锌中某些物质及稀硫酸构成原电池,所以锌中含有杂质;
原电池能加快负极金属的腐蚀速率,所以如果使用纯锌,其他条件相同,打开K和关闭K产生气泡速率较快的是关闭K时产生气泡较快,
故答案为:锌片不纯,含杂质的锌片在稀硫酸中构成原电池;关闭K时产生气泡较快.
点评:本题采用对比实验的方法探究原电池原理,根据两个对比实验确定原电池电极上发生的反应,原电池中电池反应和活泼金属与电解质溶液反应相同,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列关于元素周期表的说法中,错误的是( )
| A、元素周期表是元素按原子序数从小到大排列而成的 |
| B、元素原子的电子层数等于其所在周期的周期序数 |
| C、四、五、六周期中都含有18种元素 |
| D、元素周期表中有18列、16个族 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol CH3+(碳正离子)中含有电子数为10NA |
| B、常温常压下,17g NH3中含有原子数4NA |
| C、常温常压下,22.4L水中含有的共价键数为2NA |
| D、在密闭容器中,1mol N2与3mol H2在一定条件下充分反应,生成氨气的分子数为2NA |
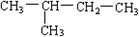 ⑧
⑧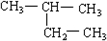
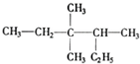
 ?2,2-二甲基丁烷.
?2,2-二甲基丁烷.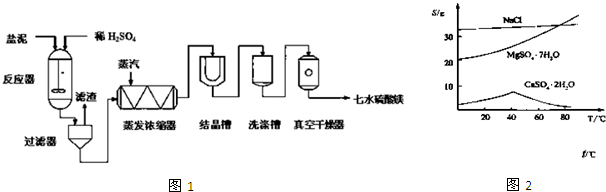
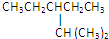
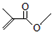 的分子式:
的分子式: