题目内容
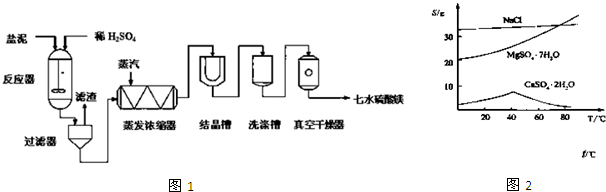
“盐泥”是粗盐提纯及电解食盐水过程中形成的工业“废料”.某工厂的盐泥含有NaCl(15~20%)、Mg(OH)2(15~20%)、CaCO3(5~10%)、BaSO4(30~40%)和不溶于酸的物质(10~15%),为了生产七水硫酸镁,设计了如图1工艺流程:
(1)电解食盐水前,为除去食盐水中的Mg2+、Ca2+、SO42-等杂质离子,下列试剂加入的先后顺序合理的是 (填序号).
A.碳酸钠、氢氧化钠、氯化钡 B.碳酸钠、氯化钡、氢氧化钠
C.氢氧化钠、碳酸钠、氯化钡 D.氯化钡、氢氧化钠、碳酸钠
(2)设食盐水中Mg2+的浓度为0.06mol?L-1,则加入氢氧化钠溶液后使溶液的pH≥ 才会产生Mg(OH)2沉淀.(Ksp[Mg(OH)2]=6.0×10-12)
(3)反应器中发生两个转化,写出其中一个反应的化学方程式: .
(4)三种化合物的溶解度(S)随温度变化曲线见图2,在过滤器中需要趁热过滤,其主要原因是 ;
滤渣的主要成分有不溶于酸的物质、 和 .
(5)在蒸发浓缩器中通入高温水蒸汽并控制温度在100~110℃,蒸发结晶,此时析出的晶体主要是 .
(6)洗涤槽中洗涤晶体的目的是除去晶体表面的杂质,检验晶体表面的Cl-已洗涤干净的方法是 .

(1)电解食盐水前,为除去食盐水中的Mg2+、Ca2+、SO42-等杂质离子,下列试剂加入的先后顺序合理的是
A.碳酸钠、氢氧化钠、氯化钡 B.碳酸钠、氯化钡、氢氧化钠
C.氢氧化钠、碳酸钠、氯化钡 D.氯化钡、氢氧化钠、碳酸钠
(2)设食盐水中Mg2+的浓度为0.06mol?L-1,则加入氢氧化钠溶液后使溶液的pH≥
(3)反应器中发生两个转化,写出其中一个反应的化学方程式:
(4)三种化合物的溶解度(S)随温度变化曲线见图2,在过滤器中需要趁热过滤,其主要原因是
滤渣的主要成分有不溶于酸的物质、
(5)在蒸发浓缩器中通入高温水蒸汽并控制温度在100~110℃,蒸发结晶,此时析出的晶体主要是
(6)洗涤槽中洗涤晶体的目的是除去晶体表面的杂质,检验晶体表面的Cl-已洗涤干净的方法是
考点:粗盐提纯
专题:实验题
分析:(1)根据除去钙离子用碳酸根离子进行沉淀,除去镁离子用氢氧根离子进行沉淀,除去硫酸根离子用钡离子沉淀,过量的钡离子需要用碳酸根离子除去进行分析;
(2)根据氢氧化镁的溶度积表达式计算出氢氧根离子浓度,再计算出溶液的pH;
(3)盐泥中的碳酸钙、氢氧化镁分别与稀硫酸反应;
(4)根据图2中温度对CaSO4?2H2O晶体的影响分析原因;滤渣中含有硫酸钡和硫酸钙等物质;
(5)根据温度对氯化钠、硫酸镁、硫酸钙晶体的影响判断析出的主要成分;
(6)检验氯离子通常使用硝酸银溶液,不过检验氯离子前需要除去干扰离子硫酸根离子.
(2)根据氢氧化镁的溶度积表达式计算出氢氧根离子浓度,再计算出溶液的pH;
(3)盐泥中的碳酸钙、氢氧化镁分别与稀硫酸反应;
(4)根据图2中温度对CaSO4?2H2O晶体的影响分析原因;滤渣中含有硫酸钡和硫酸钙等物质;
(5)根据温度对氯化钠、硫酸镁、硫酸钙晶体的影响判断析出的主要成分;
(6)检验氯离子通常使用硝酸银溶液,不过检验氯离子前需要除去干扰离子硫酸根离子.
解答:
解:(1)加入的钡离子可以由碳酸钠除去,故最后加碳酸钠,钡试剂与氢氧化钠先后都可,故加入试剂的顺序为先加NaOH,后加钡试剂,再加Na2CO3或先加钡试剂,后加NaOH,再加Na2CO3,所以D正确,
故答案为:D;
(2)根据氢氧化镁的溶度积表达式可知,c(OH-)2=
=1×10-10,则:c(OH-)=
=1×10-5mol/L,溶液中氢离子浓度为:1×10-9mol/L,溶液的pH=9.所以溶液的pH≥9时才出现氢氧化镁沉淀,
故答案为:9;
(3)盐泥中的碳酸钙、氢氧化镁分别与硫酸反应,反应的化学方程式为:CaCO3+H2SO4=CaSO4+H2O+CO2↑、Mg(OH)2+H2SO4=MgSO4+2H2O,
故答案为:CaCO3+H2SO4=CaSO4+H2O+CO2↑或Mg(OH)2+H2SO4=MgSO4+2H2O;
(4)在蒸发浓缩的过程中,温度大于40℃时随温度升高CaSO4?2H2O晶体溶解度降低,故会析出CaSO4?2H2O晶体,且应该趁热过滤,防止温度降低CaSO4?2H2O的溶解度变大,又重新溶解,不利于钙盐和镁盐的分离;同时温度降低硫酸镁晶体会析出,造成产量损失;滤渣的主要成分有不溶于酸的物质、盐泥中含有的硫酸钡,蒸发酒精出来的硫酸钙,
故答案为:温度较高时钙盐与镁盐分离更彻底(或高温下CaSO4?2H2O溶解度小);硫酸钡(BaSO4); 硫酸钙(CaSO4或CaSO4?2H2O);
(5)根据图象可知,在蒸发浓缩器中通入高温水蒸汽并控制温度在100~110℃蒸发结晶,CaSO4?2H2O的溶度积非常小,此时析出的晶体主要是:氯化钠,
故答案为:氯化钠(NaCl);
(6)滤液中的硫酸根离子会影响氯离子的干扰,应该先除去硫酸根离子,再检验氯离子,方法为:取最后洗涤液少许于试管中,滴加Ba(NO3)2溶液至不再产生沉淀,静置(1分),向上层清液滴加硝酸酸化的AgNO3溶液,无沉淀产生.
故答案为:取最后洗涤液少许于试管中,滴加Ba(NO3)2溶液至不再产生沉淀,静置,向上层清液滴加硝酸酸化的AgNO3溶液,无沉淀产生.
故答案为:D;
(2)根据氢氧化镁的溶度积表达式可知,c(OH-)2=
| 6.0×10-12 |
| 0.06 |
| 1×10-10 |
故答案为:9;
(3)盐泥中的碳酸钙、氢氧化镁分别与硫酸反应,反应的化学方程式为:CaCO3+H2SO4=CaSO4+H2O+CO2↑、Mg(OH)2+H2SO4=MgSO4+2H2O,
故答案为:CaCO3+H2SO4=CaSO4+H2O+CO2↑或Mg(OH)2+H2SO4=MgSO4+2H2O;
(4)在蒸发浓缩的过程中,温度大于40℃时随温度升高CaSO4?2H2O晶体溶解度降低,故会析出CaSO4?2H2O晶体,且应该趁热过滤,防止温度降低CaSO4?2H2O的溶解度变大,又重新溶解,不利于钙盐和镁盐的分离;同时温度降低硫酸镁晶体会析出,造成产量损失;滤渣的主要成分有不溶于酸的物质、盐泥中含有的硫酸钡,蒸发酒精出来的硫酸钙,
故答案为:温度较高时钙盐与镁盐分离更彻底(或高温下CaSO4?2H2O溶解度小);硫酸钡(BaSO4); 硫酸钙(CaSO4或CaSO4?2H2O);
(5)根据图象可知,在蒸发浓缩器中通入高温水蒸汽并控制温度在100~110℃蒸发结晶,CaSO4?2H2O的溶度积非常小,此时析出的晶体主要是:氯化钠,
故答案为:氯化钠(NaCl);
(6)滤液中的硫酸根离子会影响氯离子的干扰,应该先除去硫酸根离子,再检验氯离子,方法为:取最后洗涤液少许于试管中,滴加Ba(NO3)2溶液至不再产生沉淀,静置(1分),向上层清液滴加硝酸酸化的AgNO3溶液,无沉淀产生.
故答案为:取最后洗涤液少许于试管中,滴加Ba(NO3)2溶液至不再产生沉淀,静置,向上层清液滴加硝酸酸化的AgNO3溶液,无沉淀产生.
点评:本题主要考查了盐的性质、除杂的方法和原则,除去多种杂质时,要考虑加入试剂的顺序,为了保证将杂质除尽,所加试剂必须过量,因此为了不引进新的杂质,后面加入的试剂要能够除去前面所进入的过量试剂.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、稀硫酸与氢氧化钡反应Ba2++SO42-═BaSO4↓ |
| B、氨水与氯化铝溶液反应Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| C、铁粉与稀盐酸反应Fe+6H+═Fe3++3H2↑ |
| D、氯气通入碘化钾溶液中Cl2+I-═Cl-+I2 |
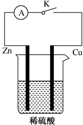 某同学为了探究原电池产生电流的过程,设计了如图所示实验.
某同学为了探究原电池产生电流的过程,设计了如图所示实验. 和
和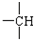 等结合成的.如果某烷分子中同时存在这4种基团,所含碳原子数最小,这种烷烃分子应含
等结合成的.如果某烷分子中同时存在这4种基团,所含碳原子数最小,这种烷烃分子应含