题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol CH3+(碳正离子)中含有电子数为10NA |
| B、常温常压下,17g NH3中含有原子数4NA |
| C、常温常压下,22.4L水中含有的共价键数为2NA |
| D、在密闭容器中,1mol N2与3mol H2在一定条件下充分反应,生成氨气的分子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.碳正离子中含有8个电子,1mol碳正离子中含有8mol电子;
B.17个氨气的物质的量为1mol,含有4mol原子;
C.常温常压下,不是标况下,且标况下水不是气体,无法计算22.4L水的物质的量;
D.氮气与氢气的反应为可逆反应,反应物不可能完全转化成生成物.
B.17个氨气的物质的量为1mol,含有4mol原子;
C.常温常压下,不是标况下,且标况下水不是气体,无法计算22.4L水的物质的量;
D.氮气与氢气的反应为可逆反应,反应物不可能完全转化成生成物.
解答:
解:A.1molCH3+(碳正离子)中含有8mol电子,含有电子数为8NA,故A错误;
B.17g NH3的物质的量为1mol,1mol氨气中含有4mol原子,含有原子数4NA,故B正确;
C.常温常压下,22.4L水的物质的量不是1mol,故C错误;
D.1mol氮气与3mol氢气生成的氨气的物质的量一定小于2mol,生成氨气的分子数小于2NA,故D错误;
故选B.
B.17g NH3的物质的量为1mol,1mol氨气中含有4mol原子,含有原子数4NA,故B正确;
C.常温常压下,22.4L水的物质的量不是1mol,故C错误;
D.1mol氮气与3mol氢气生成的氨气的物质的量一定小于2mol,生成氨气的分子数小于2NA,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项A为易错点,注意CH3+与甲基、氢氧根离子与羟基中含有的电子数.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列粒子(或化学键)的数目之比不是1:1的是( )
| A、氘原子中的质子和中子 |
| B、Na2O2固体中的阴离子和阳离子 |
| C、CO2分子中的σ键和π键 |
| D、常温下,pH=7的CH3COOH与CH3COONa混合溶液中的H+与OH- |
下列各组元素原子中,按金属性依次增强或非金属性依次减弱的是( )
| A、Na,Mg,Al |
| B、N,O,F |
| C、Li,Na,K |
| D、Cl,I,Br |
下列各组物质,不用任何化学试剂,只需用相互反应的方法就能够鉴别的是( )
| A、盐酸、Na2CO3溶液、NaCl溶液、AgNO3溶液 |
| B、Cl2、HCl、HBr |
| C、BaCl2溶液、NaOH溶液、AgNO3溶液、NaCl溶液 |
| D、NaCl溶液、NaBr溶液、NaI溶液 |
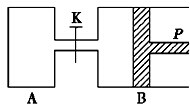 如图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入2mol X、2mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达到平衡时,VB=0.6a L.下列说法错误的是( )
如图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入2mol X、2mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达到平衡时,VB=0.6a L.下列说法错误的是( )| A、B中X的转化率为75% |
| B、A中X的转化率比B中的低 |
| C、平衡时A中混合气体密度比B小 |
| D、打开K,一段时间后反应再次达到平衡,则B的体积为1.2a L |
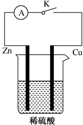 某同学为了探究原电池产生电流的过程,设计了如图所示实验.
某同学为了探究原电池产生电流的过程,设计了如图所示实验.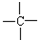 和
和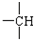 等结合成的.如果某烷分子中同时存在这4种基团,所含碳原子数最小,这种烷烃分子应含
等结合成的.如果某烷分子中同时存在这4种基团,所含碳原子数最小,这种烷烃分子应含