题目内容
17.从海水中提取镁,主要步骤如图所示:下列说法不正确的是( )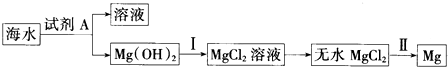
| A. | 试剂A为石灰乳,价格低廉,可来自贝壳 | |
| B. | 操作Ⅰ中加入的试剂为盐酸 | |
| C. | 以上提取镁的过程中没有涉及氧化还原反应 | |
| D. | 操作Ⅱ的条件为电解 |
分析 海水中加入石灰乳,主要是沉淀海水中的镁离子生成氢氧化镁沉淀,过滤后得到的氢氧化镁加入盐酸溶解后得到溶液,浓缩蒸发,冷却结晶,过滤得到氯化镁晶体,在氯化氢气流中加热得到氯化镁固体,电解熔融氯化镁得到镁和氯气,据此分析选项.
解答 解:A、试剂A为石灰乳,价格低廉,可来自贝壳,碳酸钙煅烧生成氧化钙,氧化钙溶于水生成氢氧化钙,故A正确;
B、操作Ⅰ是溶解氢氧化镁沉淀制备氯化镁溶液,加入试剂不能引入其它杂质,需要加入盐酸,故B正确;
C、电解氯化镁生成氯气和镁,属于氧化还原反应,故C错误;
D、电解熔融氯化镁得到镁和氯气,操作Ⅱ的条件为电解,故D正确;
故选C.
点评 本题考查海水的综合利用分析判断,题目难度中等,注意镁的提取过程和分液实质理解应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.某同学弄清氨的喷泉实验原理后有了一个创新的设计:如果改换烧瓶内的气体和胶头滴管与烧杯中的液体,也能做成喷泉实验.下列各组中的气体和液体不符合该学生设计的一组是( )
| A. | HCl和水 | B. | CO2和NaOH溶液 | C. | NO和水 | D. | Cl2和NaOH溶液 |
5.下列有关化学用语表示正确的是( )
| A. | 四氯化碳分子比例模型: | B. | COS的电子式是: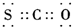 | ||
| C. | 次氯酸的结构式为H-Cl-O | D. | ${\;}_{8}^{18}$O2-离子结构示意图: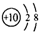 |
12.X、Y、Z、W、M均为短周期元素且原子序数依次增大,X、M同主族;Z+、W3+与Y2-具有相同的电子层结构;M 是地壳中含量占第二的元素.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | B. | 粒子半径:r(W3+)>r(Y2-)>r(Z+) | ||
| C. | MY2与Z2Y的化合物类型相同 | D. | 单质沸点:M>Z>Y |
2.以下化学反应的离子方程式书写正确的是( )
| A. | H2CO3电离:H2CO3?2H++CO32- | |
| B. | 将少量金属钠放入冷水中:Na+2H2O═Na++2OH-+H2↑ | |
| C. | C12溶解于水:H2O+Cl2?2H++ClO-+Cl- | |
| D. | 向CuSO4溶液中通入H2S:Cu2++H2S═CuS↓+2H+ |
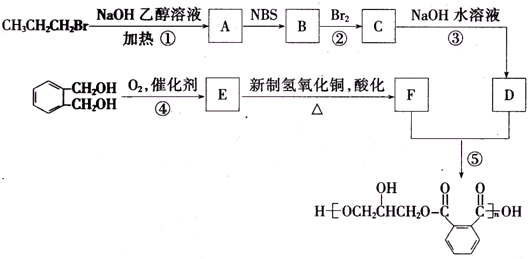
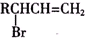
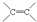 ,C的名称是1,2,3-三溴丙烷.
,C的名称是1,2,3-三溴丙烷. ;
;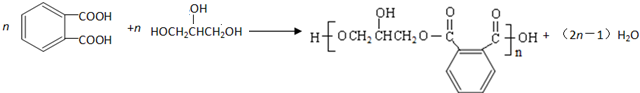 .
. 的同分异构体的结构简式
的同分异构体的结构简式 .
.



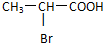 ;
;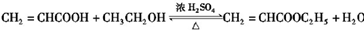 ,该反应的反应类型为酯化反应(或取代反应);
,该反应的反应类型为酯化反应(或取代反应);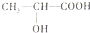 ,试写出C与金属Na反应的化学方程式为:
,试写出C与金属Na反应的化学方程式为: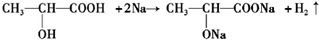 .
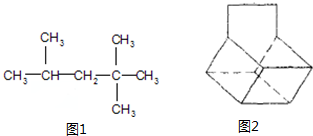
.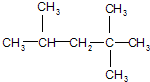 :它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷,若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3;
:它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷,若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3;