题目内容
【题目】金属材料在国民经济建设等领域具有重要应用,镁、铬、镍、铜是几种重要的金属元素。请回答下列问题:
(1)镍元素的核电荷数为28,则原子基态电子排布式为__,结构中有__种不同形状的电子云。
(2)镁属于元素周期表中的__区元素,MgO的熔点高于CuO的原因是__。
(3)氯化铬酰(CrO2Cl2)熔点:-96.5℃,沸点:117℃,能与CS2等互溶,则固态CrO2Cl2属于__晶体。已知NO2+与CS2互为等电子体,则1molNO2+中含有π键数目为__。
(4)配合物[Cu(CH3C≡N)4]BF4中碳原子杂化轨道类型为__,[Cu(CH3C≡N)4]+中所有元素的电负性由大到小的顺序是__,BF4-的空间构型为__。
(5)铜与氧元素可形成如图所示的晶胞结构,其中Cu均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(![]() ,
,![]() ,
,![]() ),则d的坐标参数为__,已知该品体的密度为ρg/cm3,NA是阿伏加德罗常数值,则晶胞参数(晶胞棱长)为__cm(列出计算式即可)。
),则d的坐标参数为__,已知该品体的密度为ρg/cm3,NA是阿伏加德罗常数值,则晶胞参数(晶胞棱长)为__cm(列出计算式即可)。


【答案】1s22s32p63s23p63d84s2(或Ar[3d84s2]) 3 s MgO的晶格能比CuO大 分子 2NA sp、sp3 N>C>H>Cu 正四面体 (![]() ,
,![]() ,
,![]() )
) ![]()
【解析】
(1)根据核外电子的排布规律书写镍的基态原子的电子排布式;不同能层的同种能级的原子轨道形状相同,据此分析判断;
(2)根据外围电子排布判断;比较离子晶体的熔点时,要看晶格能的大小,晶格大,熔点高,反之,熔点低;
(3)分子晶体的熔沸点较低;二硫化碳和NO2+的结构相似,根据二硫化碳的结构确定NO2+中π键个数;
(4)①根据价层电子对个数=σ键个数+孤电子对个数,确定微粒的空间构型和原子的杂化方式;同周期元素,从左到右元素的电负性增强,金属的电负性最弱;
(5)根据a、b点的坐标参数分析d点的坐标参数;根据均摊法计算原子数,再利用ρ=![]() 计算晶胞参数。
计算晶胞参数。
(1)镍为28号元素,根据核外电子的排布规律,先排4s能级,再排3d能级,故镍的基态原子的电子排布式为1s22s22p63s23p63d84s2(或[Ar]3d84s2),有s、p、d三种轨道,故有3种不同形状的电子云,故答案为:1s22s22p63s23p63d84s2(或[Ar]3d84s2);3;
(2) 镁的外围电子排布为3s2,在元素周期表中位于s区;MgO和CuO均为离子晶体,所含离子所带的电荷数相同,但Mg2+半经比Cu2+半径小,故MgO的晶格能大,熔点高,故答案为:s;Mg2+半径比Cu2+半径小,MgO的晶格能比CuO大;
(3)分子晶体的熔沸点较低,氯化铬酰的熔沸点较低,所以氯化铬酰属于分子晶体;二硫化碳和NO2+互为等电子体,结构相似,根据二硫化碳的结构知NO2+中有2个π键,所以1molNO2+中含有π键数目为2NA,故答案为:分子;2NA;
(4) 配合物[Cu(CH3C≡N)4]BF4的-CH3中C形成4个σ键,无孤电子对,中心C原子为sp3杂化,-C≡N中C形成2个σ键,无孤电子对,中心C原子为sp杂化;[Cu(CH3C≡N)4]+离子中涉及元素分别为C、H、N、Cu,同周期自左而右,电负性增大,电负性N>C,H元素与C、N元素化合时,H元素表现正化合价,H元素的电负性比C、N元素小,金属的电负性最弱,故电负性N>C>H>Cu,BF4-的价层电子对数=4+![]() =4,无孤电子对,故空间构型为正四面体形,故答案为:sp、sp3杂化;N>C>H>Cu;正四面体;
=4,无孤电子对,故空间构型为正四面体形,故答案为:sp、sp3杂化;N>C>H>Cu;正四面体;
(5)根据a(0,0,0)、b(![]() ,
,![]() ,
,![]() )的坐标参数,可分析d点坐标参数为(
)的坐标参数,可分析d点坐标参数为(![]() span>,
span>,![]() ,
,![]() );晶胞中O的个数为8×
);晶胞中O的个数为8×![]() +1=2,Cu的个数为4,则晶胞质量为
+1=2,Cu的个数为4,则晶胞质量为![]() g,ρ=
g,ρ=![]() =
=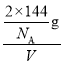 ,则V=
,则V=![]() cm3,则晶胞参数a=
cm3,则晶胞参数a=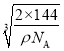 cm,故答案为:(
cm,故答案为:(![]() ,
,![]() ,
,![]() ) ;
) ;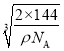 。
。