题目内容
【题目】电化学降解法可用于治理水中硝酸盐的污染,电化学降解NO3-的原理如图所示,下列说法正确的是
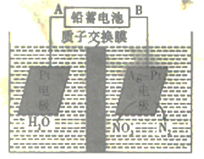
A.电源正极为B
B.H+由右侧通过交换膜移动到左侧
C.该电解池的阴极反应式为2NO3-+12H+ +10e-=N2↑+6H2O
D.标况下,若有2. 24LN2生成,理论上铅蓄电池中有20.7克Pb消耗
【答案】C
【解析】
图中信息为:在Ag-Pt电极上,NO3-→N2,N元素由+5价降低为0价,则此电极为阴极,Pt电极为阳极。
A.B电极与阴极相连,则B电极为电源负极,A不正确;
B.在阳极,2H2O-4e-=O2↑+4H+,H+由左侧通过交换膜移动到右侧,B不正确;
C.在电解池的阴极,NO3-在酸性溶液中得电子生成N2和H2O,反应式为2NO3-+12H+ +10e-=N2↑+6H2O,C正确;
D.标况下,若有2. 24LN2生成,则转移电子1mol,理论上铅蓄电池中消耗Pb 0.5mol×207g/mol=103.5g,D不正确;
故选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目