题目内容
3.下列说法不正确的是( )| A. | 二氧化氮会导致酸雨和光化学烟雾,危害较大 | |
| B. | 铝制品不宜用于盛放酸、碱溶液,不宜长时间盛放咸菜等腌制食品 | |
| C. | 人体中极少量的NO 会促进血管扩张,防止血管栓塞 | |
| D. | 利用铝热反应可实现工业制镁 |
分析 A.光化学烟雾形成的重要原因是汽车尾气排放的氮氧化物,同时氮氧化物会转变成硝酸,造成酸雨;
B.氯化钠也会破坏氧化膜的结构;
C.NO作为信号分子,使血管扩张而帮助控制血液流向人体的各个部位;
D.工业制镁用电解法.
解答 解:A.汽车尾气中含有氮氧化物,大量排放不仅会造成酸雨还可能导致光化学烟雾,故A正确;
B.氧化铝虽然为致密的氧化物薄膜,但氯化钠也会破坏氧化膜的结构,从而加速铝制品的腐蚀,故B正确;
C.NO是明星分子,在人体的血管系统内具有传送信号的功能,NO极少量时在人体的血管系统内会促进血管扩张,防止血管栓塞,故C正确;
D.铝性质较活泼,工业制镁用电解法,故D错误.
故选D.
点评 本题考查较综合,侧重考查化学在生产生活中的应用,注重基础知识的考查,题目难度不大,注意相关知识的积累.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
13.下列说法正确的是( )
| A. | 淀粉和纤维素的分子式都是(C6H10O5)n,所以它们都是同分异构体. | |
| B. | 糖类都是有甜味的物质 | |
| C. | 鉴别织物成分是真丝还是人造丝可以用灼烧的方法. | |
| D. | 蔗糖水解前后都可以发生银镜反应 |
14.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水反应的化学方程式是:4K2FeO4+10H2O═4Fe(OH)3(胶体)+3O2↑+8KOH工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入一定量的KOH就可制得高铁酸钾.制备高铁酸钠的两种方法的主要反应原理如下:
湿法制备:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O
干法制备:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法中错误的是( )
湿法制备:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O
干法制备:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法中错误的是( )
| A. | 高铁酸钾处理水时,水发生氧化反应 | |
| B. | 湿法中每生成1mol Na2FeO4共转移3mol电子 | |
| C. | 干法中每生成1mol Na2FeO4共转移3mol电子 | |
| D. | K2FeO4处理水时,不仅能杀菌,并能使悬浮杂质沉降 |
11.已知氮化铝的晶胞结构如图所示,下列说法正确的是( )


| A. | 氮化铝晶胞结构与NaCl相同 | B. | 第一电离能N<Al | ||
| C. | 电负性N>Al | D. | 原子半径N>Al |
18.下列不是海水淡化主要方法的是( )
| A. | 蒸馏法 | B. | 离子交换法 | C. | 电渗析法 | D. | 干馏法 |
8.常温下在水中加入下列物质,不会破坏水的电离平衡的是( )
| A. | 通入HCl 气体 | B. | 加入NaOH 固体 | C. | 加入蔗糖 | D. | 加入金属钠 |
15.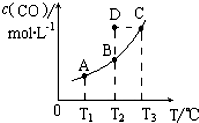 在恒容密闭容器中存在下列平衡:C(s)+H2O(g)?CO(g)+H2(g)的平衡物质的量浓度与温度 T的关系如图所示.下列说法错误的是( )
在恒容密闭容器中存在下列平衡:C(s)+H2O(g)?CO(g)+H2(g)的平衡物质的量浓度与温度 T的关系如图所示.下列说法错误的是( )
 在恒容密闭容器中存在下列平衡:C(s)+H2O(g)?CO(g)+H2(g)的平衡物质的量浓度与温度 T的关系如图所示.下列说法错误的是( )
在恒容密闭容器中存在下列平衡:C(s)+H2O(g)?CO(g)+H2(g)的平衡物质的量浓度与温度 T的关系如图所示.下列说法错误的是( )| A. | 该反应的△H>0 | |
| B. | 若T1、T2 时的平衡常数分别为K1、K2,则K1=K2 | |
| C. | 通过加热可以使B 点变到C 点 | |
| D. | 在T2时若反应进行到状态D,则一定有υ(正)<υ(逆) |
12.已知常温下,0.1mol•L?1CH3COONH4溶液呈中性.下列有关叙述正确的是( )
| A. | 该溶液可由等体积、浓度均为0.1mol•L?1的醋酸和氨水反应得到 | |
| B. | CH3COONH4加入纯水中,水的电离程度不变 | |
| C. | 常温下,电离常数K(CH3COOH)=K(NH3•H2O) | |
| D. | 该溶液中c(CH3COO?)大于同浓度CH3COONa溶液中的c(CH3COO?) |
13.某二元酸H2A电离方程式是:H2A=H++HA-,HA-?A2-+H+,下列说法正确的( )
| A. | 无法确定NaHA溶液的酸碱性 | |
| B. | NaHA溶液中:c(H+)=c(A2-)+c(OH-) | |
| C. | 若0.1mol/L NaHA溶液的pH=2,则0.1mol/L H2A溶液中c(H+)=0.11mol/L | |
| D. | 常温下1mol/L NaHA溶液与1mol/L NaOH溶液等体积混合所得溶液pH=7 |