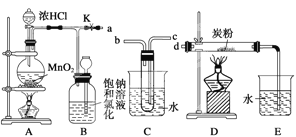
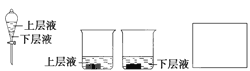
��Ŀ����
����Ŀ�������ܽ�����п�̻���ȡ�ߴ�п�Ĺ���������ͼ��ʾ���ܽ�������п�̻���п��ͭ���ӡ���Ԫ�طֱ���Zn(NH3)42+��Cu(NH3)42+��Cd(NH3)42+��AsCl52������ʽ���ڡ�
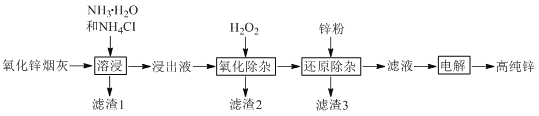
ע�����������ӡ��У�AsCl52��ת��ΪAs2O5���������۳���ȥ����Һʼ�սӽ����ԡ�
�ش��������⣺
��1��Zn(NH3)42+��Zn�Ļ��ϼ�Ϊ________�����ܽ�����ZnO������Ӧ�����ӷ���ʽΪ________��
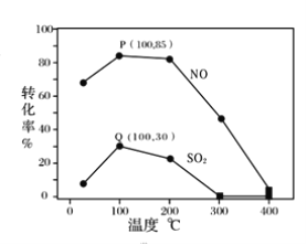
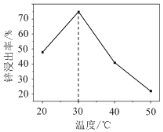
��2��п���������¶ȵĹ�ϵ��ͼ��ʾ������30 ��ʱп��������ߵ�ԭ��Ϊ________��
��3��������3������Ҫ�ɷ�Ϊ________��
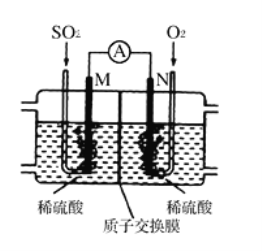
��4������⡱ʱZn(NH3)42+�������ŵ�ĵ缫��ӦʽΪ_______���������ų�һ����ɫ��ζ�����壬����ͨ�����KSCN��FeCl2��Һ�У�����������������________��д��ѧʽ��������ĵ��Һ������________��дһ�����ʵĻ�ѧʽ����ɷ��ء��ܽ����������ʹ�á�
���𰸡�+2 ZnO+2NH3��H2O+2NH4+=Zn(NH3)42++3 H2O ����30��ʱ���ܽ���Ӧ�������¶����߶�������30�棬�����ݳ������ܽ���Ӧ�����½� Cu��Cd Zn(NH3)42++2e-=Zn+4 NH3����Zn(NH3)42++2e-+4H2O= Zn+4NH3��H2O N2 NH3����NH3��H2O��
��������
����п�̻��м��백ˮ���Ȼ���ܽ�������п�̻���п��ͭ���ӡ���Ԫ�طֱ���Zn(NH3)42+��Cu(NH3)42+��Cd(NH3)42+��AsCl52������ʽ���ڣ�����Һ�м���˫��ˮ��AsCl52��ת��ΪAs2O5���������۳���ȥ����Һʼ�սӽ����ԣ�����п�۽�Cd��Cu�û����������˳�����������Һ����ҪΪZn(NH3)42+�����Ϳɵõ��ߴ�п��
��1��Zn(NH3)42+��Zn�Ļ��ϼ�Ϊ+2�ۣ������ܽ�����ZnO�백ˮ������Ӧ����Zn(NH3)42+�����ӷ���ʽ�� ZnO+2NH3��H2O+2NH4+=Zn(NH3)42++3H2O ��
�𰸣�+2 ZnO+2NH3��H2O+2NH4+=Zn(NH3)42++3H2O
��2���¶�Խ�ߣ���Ӧ��Ũ��Խ��ѧ��Ӧ����Խ�죬������ҲԽ�ߣ���ˮ���ȶ������ֽ��ݳ�������
�𰸣�����30��ʱ���ܽ���Ӧ�������¶����߶�������30�棬�����ݳ������ܽ���Ӧ�����½�
��3������п�۽�Cd��Cu�û����������˳�����������Һ����ҪΪZn(NH3)42+������������Cd��Cu��
�𰸣� Cu��Cd
��4�������Ҫ��õ��ߴ�п���������Zn(NH3)42+�õ�������п������ʧ���ӷų�һ����ɫ��ζ�����壬����ͨ�����KSCN��FeCl2��Һ�У�����������˵������������ʧ���ӻ��ϼ������ߵ�ֻ��NԪ�شӸ��������ߵ�0�ۣ�����N2��������Zn(NH3)42++2e-=Zn+4NH3��������:2NH3��H2O-6e-=N2+2H2O+6H+,����ĵ��Һ���� NH3����NH3��H2O����ɷ��ء��ܽ����������ʹ�á�
�𰸣�Zn(NH3)42++2e-=Zn+4NH3����Zn(NH3)42++2e-+4H2O=Zn+4NH3��H2O N2 NH3����NH3��H2O��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�