题目内容
【题目】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O===Se+2SO42—+4H+。
(1) Se与浓H2SO4的反应中,氧化剂是________________,还原剂是_______________。当有标准状况下22.4 L SO2气体生成时,转移电子的物质的量是________ mol。
(2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是______________________。
(3)用单线桥法标出反应②电子转移的方向和数目:_____________________________。
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3―→Se+I2+KNO3+H2O配平上述反应的化学方程式______________________________________________。
【答案】浓硫酸(或H2SO4) 硒(或Se) 2 浓硫酸>二氧化硒>二氧化硫 或H2SO4>SeO2>SO2  SeO2+4KI+4HNO3===Se+2I2+4KNO3+2H2O
SeO2+4KI+4HNO3===Se+2I2+4KNO3+2H2O
【解析】
(1)所含元素化合价降低的物质是氧化剂,所含元素化合价升高的物质是还原剂,根据硫元素的化合价变化情况计算转移电子的物质的量;
(2)根据氧化剂的氧化性强于氧化产物的氧化性分析解答;
(3)根据电子得失守恒分析解答;
(4)根据电子得失守恒和原子守恒配平方程式。
(1)氧化剂是化合价降低物质,根据反应方程式,H2SO4中S由+6价→+4价,化合价降低,即H2SO4是氧化剂,还原剂是化合价升高的物质,Se的化合价由0价→+4价,化合价升高,Se为还原剂;标准状况下22.4 L SO2气体的物质的量是1.0mol,硫元素化合价降低2价,则转移电子物质的量为2mol;
(2)利用氧化剂的氧化性强于氧化产物的氧化性可知,①中得出H2SO4的氧化性强于SeO2,②中SeO2是氧化剂,SO2体现还原性,因此SeO2的氧化性强于SO2,综上所述氧化性强弱顺序为浓硫酸>二氧化硒>二氧化硫;
(3)反应②中SO2中S的化合价由+4价→+6价,升高2价,2molSO2共失去4mol电子,SeO2中Se由+4价→0价,化合价降低4价,因此单线桥表示为 ;
;
(4)SeO2中Se元素化合价由+4价→0价,化合价降低4价,KI中I元素化合价由-1价→0价,化合价升高1价,最小公倍数为4,因此有SeO2+4KI+HNO3→Se+2I2+KNO3+H2O,然后根据原子守恒配平其他物质的系数,即反应方程方式为SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O。

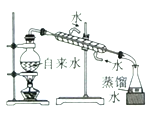
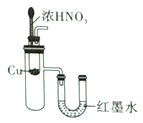
【题目】下列实验装置不能达到实验目的的是
A | B | C | D |
|
|
|
|
实验室制取蒸馏水 | 用SO2和NaOH溶液做喷泉实验 | 证明Na2CO3的热稳定性比NaHCO3好 | 证明铜与浓硝酸的反应是放热反应 |
A. A B. B C. C D. D