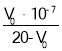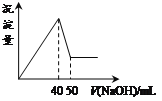题目内容
【题目】某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为 45.3g 的该结晶水合物,分别制成溶液向其中一份逐滴加入 NaOH 溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出, 该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到 2.24L 该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入 Ba(OH)2 溶液,开始现象类似,但最终仍有白色沉淀; 过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体 46.6g。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是_____和_____,阴离子是_____;
(2)试通过计算确定该结晶水合物的化学式。写出计算过程:_____假设过程中向该溶液中加入的 Ba(OH)2 溶液的物质的量浓度为 2.0molL1 。
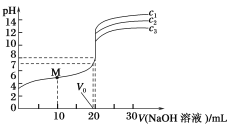
(3)加入_____mLBa(OH)2 溶液时,所得沉淀的总物质的量最大。
(4)请在如图中画出生成沉淀的物质的量与加入 Ba(OH)2 溶液体积的关系示意图_____。

【答案】NH4+ Al3+ SO42- NH4Al(SO4)212H2O[或(NH4)2SO4Al2(SO4)324H2O] 100 
【解析】
(1)一份加入NaOH溶液,一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,该气体是氨气,明一定含有铵根离子;向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多,最后白色沉淀逐渐减少并最终消失,证明一定含有铝离子,一份加入足量Ba(OH)2溶液,生成白色沉淀,过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6g,说明含有硫酸根离子;故答案为:NH4+;Al3+;SO42-;
(2)由题中信息可知45.3g的该结晶水合物中:n(SO42-)=![]() ,n(NH4+)=
,n(NH4+)=![]() ,根据离子化合物中阴、阳离子电荷平衡的原理:n(NH4+)+3n(Al3+)=2n(SO42-)可得:n(A13+)=
,根据离子化合物中阴、阳离子电荷平衡的原理:n(NH4+)+3n(Al3+)=2n(SO42-)可得:n(A13+)=![]() =0.1mol,n(H2O)=
=0.1mol,n(H2O)=![]() ,所以该结晶水合物中:n(NH4+):n(A13+):n(SO42-):n(H2O)=0.1mol:0.1mol:0.2mol:1.2mol=1:1:2:12,该结晶水合物的化学式为NH4Al(SO4)212H2O,故答案为:NH4Al(SO4)212H2O;
,所以该结晶水合物中:n(NH4+):n(A13+):n(SO42-):n(H2O)=0.1mol:0.1mol:0.2mol:1.2mol=1:1:2:12,该结晶水合物的化学式为NH4Al(SO4)212H2O,故答案为:NH4Al(SO4)212H2O;
(3)加入Ba(OH)2溶液沉淀物质的量最大,此时Al3+、Ba2+沉淀完全,则n(Ba(OH)2)= n(SO42-)==0.2mol,则V(Ba(OH)2)=![]() = 100mL,故答案为:100;
= 100mL,故答案为:100;
(4)根据反应的先后顺序,开始阶段是氢氧化钠和铝离子反应生成氢氧化铝沉淀,钡离子和硫酸根生成硫酸钡沉淀,当n(Ba(OH)2)=![]() 时,Al3+沉淀完全, 此时V(Ba(OH)2)=
时,Al3+沉淀完全, 此时V(Ba(OH)2)=![]() ,沉淀的总物质的量为:0.1mol+0.15mol=0.25mol;之后沉淀继续增加的为硫酸钡沉淀,达到最大值时,V(Ba(OH)2)=
,沉淀的总物质的量为:0.1mol+0.15mol=0.25mol;之后沉淀继续增加的为硫酸钡沉淀,达到最大值时,V(Ba(OH)2)=![]() = 100mL,沉淀的总物质的量为0.1mol+0.2mol=0.3mol;最后是氢氧化铝和氢氧化纳反应生成偏铝酸钠的阶段,此时消耗的V(Ba(OH)2)=
= 100mL,沉淀的总物质的量为0.1mol+0.2mol=0.3mol;最后是氢氧化铝和氢氧化纳反应生成偏铝酸钠的阶段,此时消耗的V(Ba(OH)2)= ,最后剩余0.2mol硫酸钡沉淀保持不变,如图示:
,最后剩余0.2mol硫酸钡沉淀保持不变,如图示:
 。
。

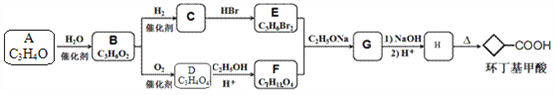
【题目】[实验化学]
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33 ~36 |
| 易溶于甲醇、乙醚,微溶于水 |
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是的_________。
②萃取用到的分液漏斗使用前需_______并洗净,分液时有机层在分液漏斗的_____填(“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是______________;用饱和食盐水洗涤的目的是______________。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_____(填字母)。
a.蒸馏除去乙醚 b..重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先_______,再______。