��Ŀ����
����Ŀ����ҵ�ϳ��Ը�������Ҫ�ɷ�Ϊ�Ǹ�������FeCr2O4��������Al2O3��SiO2�����ʣ�Ϊ��Ҫԭ�������췯�ƣ�Na2Cr2O7����ijʵ��С��ģ������������ͼ��ʾ��
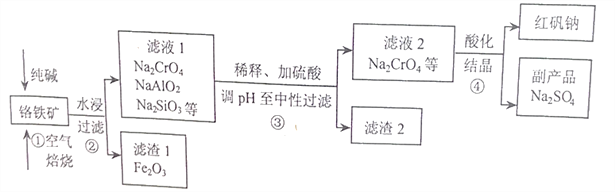
��1��FeCr2O4��Cr�Ļ��ϼ�Ϊ____________������ٱ���ʱ���õ���������Ϊ_________�������������Na2CrO4�Ļ�ѧ����ʽΪ________________________��
��2����������շ�Ӧ��������Ҫ���������������״̬����Ӧ���ʲżӿ죬����Ҫԭ��Ϊ________��
��3������ڹ���ʱ���õ��IJ���������________________��
��4������������Ὣ��Һ��pH�������ԣ���������2����Ҫ�ɷ���__________��__________��
��5�����������Һ2���������ữ�����У���Һ�ɻ�ɫ��Ϊ��ɫ����Ӧ�����ӷ���ʽΪ___________��
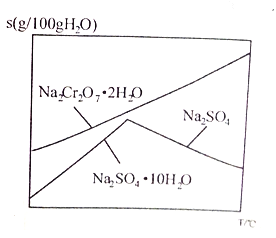
��6����ͼ��Na2Cr2O7��2H2O��Na2SO4���ܽ�����ߣ�������л�ø���ƷNa2SO4��ʵ���������Ϊ____________________��
���𰸡� +3 ���������� 4FeCrO4+7O2+ 8Na2CO3![]() 2Fe2O3+8Na2CrO4+8CO2 �����ۻ�������Ӧ��ĽӴ������ʹ��Ӧ���ʼӿ� ©�����ձ��������� H2SiO3��H4SiO3�� SiO2��H2O����Al(OH)3 2CrO42- + 2H+ = Cr2O72-+ H2O ����Һ2����Ũ������ȹ��˵ø���Ʒ Na2SO4 ��
2Fe2O3+8Na2CrO4+8CO2 �����ۻ�������Ӧ��ĽӴ������ʹ��Ӧ���ʼӿ� ©�����ձ��������� H2SiO3��H4SiO3�� SiO2��H2O����Al(OH)3 2CrO42- + 2H+ = Cr2O72-+ H2O ����Һ2����Ũ������ȹ��˵ø���Ʒ Na2SO4 ��
����������Ӧ�� 4FeCrO4+7O2�� 8Na2CO3 ![]() 2Fe2O3+8Na2CrO4+8CO2 �� NaFeO2��ˮ��Ӧ��������ɫ��������NaFeO2+2H2O=NaOH+Fe(OH)3 �������ɵ��������ƺ���������Ӧ����ƫ�����ƣ��Ͷ������跴Ӧ���ɹ����ƣ���Һ1�ijɷֳ�Na2CrO4�⣬������ƫ�����ƺ����ƣ��۵���PH�����ԣ���Һ1�к���Na2SiO3��NaAlO2������pH������Al(OH)3 ��H2SiO3����Cr2O72��+H2O
2Fe2O3+8Na2CrO4+8CO2 �� NaFeO2��ˮ��Ӧ��������ɫ��������NaFeO2+2H2O=NaOH+Fe(OH)3 �������ɵ��������ƺ���������Ӧ����ƫ�����ƣ��Ͷ������跴Ӧ���ɹ����ƣ���Һ1�ijɷֳ�Na2CrO4�⣬������ƫ�����ƺ����ƣ��۵���PH�����ԣ���Һ1�к���Na2SiO3��NaAlO2������pH������Al(OH)3 ��H2SiO3����Cr2O72��+H2O![]() 2CrO42��+2H����������Һ2�еĸ�����ת��ΪNa2Cr2O7��ҺӦ��ȡ�Ĵ�ʩ�Ǽ������ữ��
2CrO42��+2H����������Һ2�еĸ�����ת��ΪNa2Cr2O7��ҺӦ��ȡ�Ĵ�ʩ�Ǽ������ữ��
��1�����ݻ��ϼ۹��������и���Ԫ�صĻ��ϼ۴�������0��Fe��+2�ۣ�O��-2�ۣ�����FeCr2O4��CrԪ�صĻ��ϼ���+3���ʴ�Ϊ��+3������ٱ���ʱ��ԭ������Na2CO3�������ù����������������õ���������Ϊ���������� ���������FeCr2O4��������������������O2Ϊ������������ʽΪ 4FeCrO4+7O2+ 8Na2CO3![]() 2Fe2O3+8Na2CrO4+8CO2 ����2����������շ�Ӧ��������Ҫ���������������״̬�����Һ������ӽӴ��������࣬��Ӧ���ʼӿ죬ʹ��Ӧ���ʼӿ죻��3������ڹ���ʱ���õ��IJ���������©�����ձ�������������4������������Ὣ��Һ��pH�������ԣ�SiO32�D��2H2O=H2SiO3��2OH�D ��AlO2�D��2H2O
2Fe2O3+8Na2CrO4+8CO2 ����2����������շ�Ӧ��������Ҫ���������������״̬�����Һ������ӽӴ��������࣬��Ӧ���ʼӿ죬ʹ��Ӧ���ʼӿ죻��3������ڹ���ʱ���õ��IJ���������©�����ձ�������������4������������Ὣ��Һ��pH�������ԣ�SiO32�D��2H2O=H2SiO3��2OH�D ��AlO2�D��2H2O![]() Al(OH)3��OH�D ����������2����Ҫ�ɷ���H2SiO3��H4SiO3�� SiO2��H2O����Al(OH)3 ����5�����������Һ2���������ữ�����У���Һ�ɻ�ɫ��Ϊ��ɫ��������ת��ΪNa2Cr2O7��Һ��2CrO42- + 2H+ = Cr2O72-+ H2O����6�����ܽ������ͼ����ʱ���ظ����Ƶ��ܽ�����¶ȵ����߶�����Na2SO4���¶Ƚϸ�ʱ�ܽ��ȴ��С������Һ2����Ũ������ȹ��˵ø���Ʒ Na2SO4 ��
Al(OH)3��OH�D ����������2����Ҫ�ɷ���H2SiO3��H4SiO3�� SiO2��H2O����Al(OH)3 ����5�����������Һ2���������ữ�����У���Һ�ɻ�ɫ��Ϊ��ɫ��������ת��ΪNa2Cr2O7��Һ��2CrO42- + 2H+ = Cr2O72-+ H2O����6�����ܽ������ͼ����ʱ���ظ����Ƶ��ܽ�����¶ȵ����߶�����Na2SO4���¶Ƚϸ�ʱ�ܽ��ȴ��С������Һ2����Ũ������ȹ��˵ø���Ʒ Na2SO4 ��

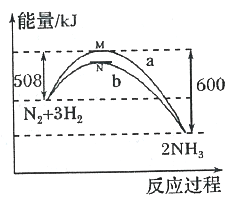
����Ŀ��ij�¶�ʱ����һ���ݻ�Ϊ2 L���ܱ������У�X��Y��Z���������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�
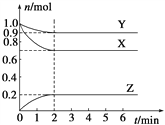
��1���÷�Ӧ�Ļ�ѧ����ʽΪ_______________��
��2����Ӧ��ʼ��2 min������Z�ķ�Ӧ����Ϊ____________��
��3����X��Y��Z��Ϊ���壬��Ӧ�ﵽƽ��ʱ��ѹǿ�ǿ�ʼʱ��________������ʱ�ų���a kJ����������1���ķ�Ӧ����ʽд���Ȼ�ѧ��Ӧ����ʽʱ���÷�Ӧ�ķ�Ӧ����H=_____________��
��4��ͨ�����ǰѲ�1 molij��ѧ�������յ��������ɸû�ѧ���ļ��ܡ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�Ħ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ��֪��
��ѧ�� | H��H | H��Cl | Cl��Cl |
����/ kJ��mol�C1 | 436 | 431 | 242 |
��ҵ��ͨ�������������г��ȼ����ȡHCl���壬д���÷�Ӧ���Ȼ�ѧ��Ӧ����ʽ��_______________��
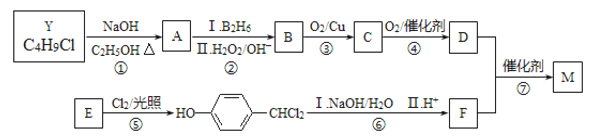
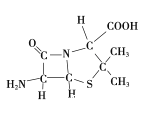
����Ŀ���������������������������ܹ��������·�Ӧ��
MnO![]() ��H2C2O4��H����Mn2����CO2����H2O(δ��ƽ)��4mL0.001mol��L��1KMnO4��Һ��2mL0.01mol��L��1H2C2O4��Һ,�о���Ӧ���¶ȡ���Ӧ���Ũ������������ضԻ�ѧ��Ӧ���ʵ�Ӱ�졣�ı�����������ʾ��
��H2C2O4��H����Mn2����CO2����H2O(δ��ƽ)��4mL0.001mol��L��1KMnO4��Һ��2mL0.01mol��L��1H2C2O4��Һ,�о���Ӧ���¶ȡ���Ӧ���Ũ������������ضԻ�ѧ��Ӧ���ʵ�Ӱ�졣�ı�����������ʾ��
��� | 10%�������/mL | �¶�/�� | �������� |
�� | 2 | 20 | |
�� | 2 | 20 | 10�α���MnSO4��Һ |
�� | 2 | 30 | |
�� | 1 | 20 | 1 mL����ˮ |
(1)�÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ________��
(2)ʵ���͢�ɵó��Ľ��ۣ�Ӱ�컯ѧ��Ӧ���ʵ�������_______������о��¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ��,ʹ��ʵ����___________(����ʾ)��
(3)ʵ����м���1 mL����ˮ��Ŀ����_______________________________��