题目内容
对于锌-铜-稀H2SO4组成的原电池装置中,当导线中有1mol电子通过时理论上的电极变化:
①锌片溶解了32.5g ②锌片增重32.5g ③铜片上析出了1g H2 ④铜片上析出1molH2
| A.①③ | B.①④ | C.②③ | D.②④ |
A
解析试题分析:对于锌-铜-稀H2SO4组成的原电池,负极Zn上发生反应:Zn-2e-=Zn2+;在正极Cu上发生反应:2H++2e-=H2↑。若导线中有1mol电子,则负极反应消耗Zn的质量是65g÷2=32.5g,质量减轻32.5g,在Cu片上产生氢气的质量是2g÷1=1g。故正确的说法是①③,选项是A。
考点:考查原电池中物质质量的变化及现象的知识。

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
如图所示的装置中,金属a能从酸中置换出H2,b为碳棒,关于此装置的各种叙述中不正确的是( )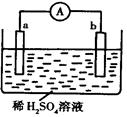
| A.碳棒上有气体放出,溶液pH值变大 |
| B.a是正极,b是负极 |
| C.导线中有电子流动,电子从a极到b极 |
| D.a极上发生了氧化反应 |
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据电镀原理,钢芯镀镍时,钢芯应该做
| A.正极 | B.负极 | C.阳极 | D.阴极 |
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是( )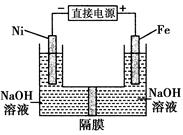
| A.铁是阳极,电极反应为Fe-6e-+4H2O===FeO+8H+ |
| B.镍电极上的电极反应为2H2O+2e-==H2↑+2OH- |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,最终溶液pH不变 |
某原电池装置如下图所示。下列有关叙述中,正确的是
A. 作正极,发生氧化反应 作正极,发生氧化反应 | B.工作一段时间后,两烧杯中溶解 均不变 均不变 |
C.负极反应: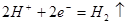 | D.工作一段时间后,NaCl溶液中c(Cl-)增大 |
下图为一原电池的结构示意图,下列说法中,错误的是 
| A.Cu电极为正电极 |
| B.原电池工作时,电子从Zn电极流出 |
| C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液 |
如下图所示,将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述中正确的是 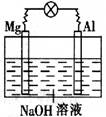
| A.镁比铝活泼,镁失去电子被氧化成Mg2+。 |
| B.铝是电池的负极,开始工作时溶液中会立即有白色沉淀生成 |
| C.该装置的内、外电路中,均是电子的定向移动形成电流 |
| D.该装置开始工作时,铝片表面的氧化膜可不必处理 |
某同学做完铜、锌稀硫酸原电池的实验后得出了下列结论,你认为正确的是
| A.构成原电池正极和负极的材料必须是两种金属 |
| B.当由铜、锌电极与硫酸铜溶液组成原电池时,铜是负极 |
| C.该实验电子沿导线由锌流向铜,氢离子得到电子而放出氢气 |
| D.铜锌原电池工作时,电流由锌经导线流向铜 |
下图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是
| A.左池电极反应式:X4+ + 2e-=X2+ |
| B.每消耗1mol Y2O72-,转移3mol电子 |
| C.改变右池溶液的c(H+),电流强度不变 |
| D.左池中阴离子数目增加 |