题目内容
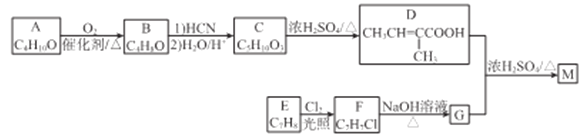
【题目】(1)有机物A中只含C、H、O三种元素,A的蒸气密度是相同状况下氢气密度的83倍,分子中碳原子总数是氧原子总数的3倍,则A的分子式为________。
(2)芳香烃B的相对分子质量在100~110之间,1 mol B充分燃烧可生成72 g水,则B的分子式是________。
(3)某含C、H、O三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是________,通过质谱仪测定其相对分子质量为74,则其分子式为________。
【答案】C9H10O3 C8H8 C4H10O C4H10O
【解析】
(1) A的蒸气密度是相同状况下氢气密度的83倍,则A的相对分子质量=2×83=166。碳原子总数是氧原子总数的3倍,设有机物的分子式为:C3xHyOx,那么有:36x+y+16x=166,因为x、y均为正整数,所以解得x1=1和y1=114(舍去)、x2=2和y2=62(舍去)、x3=3和y3=10,所以该有机物的分子式为:C9H10O3,故答案为:C9H10O3;
(3)设B的分子式为CxHy,1 mol B充分燃烧可生成72g水的物质的量=![]() =4mol,根据H原子守恒可知:y=8,分子式为:CxH8,又因为B的相对分子质量在100~110之间,x为正整数,所以,x=8,故A的分子式为:C8H8,故答案为:C8H8;
=4mol,根据H原子守恒可知:y=8,分子式为:CxH8,又因为B的相对分子质量在100~110之间,x为正整数,所以,x=8,故A的分子式为:C8H8,故答案为:C8H8;
(3)碳的质量分数是64.86%,氢的质量分数是13.51%,那么,氧的质量分数=1-64.86%-13.51%=21.63%, C、H、O的个数比=![]() :
:![]() :
:![]() ≈4:10:1,所以,该有机物的实验式为:C4H10O。相对分子质量为74,则该有机物分子式为:C4H10O,故答案为:C4H10O;C4H10O。
≈4:10:1,所以,该有机物的实验式为:C4H10O。相对分子质量为74,则该有机物分子式为:C4H10O,故答案为:C4H10O;C4H10O。

【题目】下表是某同学探究Na2SO3溶液和铬(VI)盐溶液反应规律的实验记录,已知:Cr2O72-(橙色)+ H2O![]() 2CrO42-(黄色)+ 2H+
2CrO42-(黄色)+ 2H+
序号 | a | b | 现象 | |
| 1 | 2 mL 0.05 mol·L1 K2Cr2O7溶液(pH = 2) | 3滴饱和Na2SO3溶液(pH = 9) | 溶液变绿色(含Cr3+) |
2 | 2 mL 0.1 mol·L1 K2CrO4溶液(pH = 8) | 3滴饱和Na2SO3溶液 | 溶液没有明显变化 | |
3 | 2 mL饱和Na2SO3溶液 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变黄色 | |
4 | 2 mL蒸馏水 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变成浅橙色 |
下列说法不正确的是
A. 实验1中的绿色溶液中含有SO42-
B. 实验1、2的a溶液中所含的离子种类相同
C. 向实验3溶液中继续滴加过量硫酸可使溶液变为浅橙色
D. 实验4的目的是排除稀释对溶液颜色变化造成的影响