题目内容
3.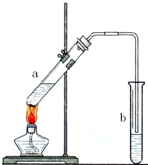 可用图示装置制取少量乙酸乙酯.已知乙酸乙酯的沸点低于乙醇.请填空:
可用图示装置制取少量乙酸乙酯.已知乙酸乙酯的沸点低于乙醇.请填空:(1)试管a中需加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序及操作是先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸.
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是在试管a中加入几粒沸石(或碎瓷片).
(3)实验中加热试管a的目的是:
①加快反应速率;
②及时将乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动.
(4)试管b中加有饱和Na2CO3溶液,其作用是吸收随乙酸乙酯蒸出的少量酸性物质和乙醇.
(5)试管b中导气管不伸入液面下的原因是防止发生倒吸.
分析 (1)浓硫酸密度大,应将浓硫酸加入到乙醇中,以防酸液飞溅,乙酸易挥发,冷却后再加入乙酸;
(2)液体加热要加碎瓷片,防止暴沸;
(3)实验中加热试管的目的提供能量;
(4)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;
(5)导管伸入液面以下会倒吸.
解答 解:(1)为防止酸液飞溅,应将密度大的液体加入到密度小的液体中,乙酸易挥发,冷却后再加入乙酸,
故答案为:先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸;
(2)液体乙酸乙醇沸点低,加热要加碎瓷片,防止暴沸,
故答案为:在试管a中加入几粒沸石(或碎瓷片);
(3)实验中加热试管,反应的温度高,反应速度快,该反应为可逆反应,温度高,乙酸乙酯的沸点低,易挥发,所以化学平衡向正反应方向移动,利于生成乙酸乙酯,
故答案为:加快反应速率;及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,
故答案为:吸收随乙酸乙酯蒸出的少量酸性物质和乙醇;
(5)导管伸入饱和碳酸钠溶液中,由于乙酸和乙醇溶于饱和碳酸钠溶液,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象;
故答案为;防止发生倒吸.
点评 本题考查了乙酸乙酯的制备,解答时须注意酯化反应的原理和饱和碳酸钠溶液的作用,题目难度不大.

练习册系列答案
相关题目
14.A、B、C、D为四种主族元素,A、B元素的阳离子和C、D元素的阴离子都具有相同的电子层结构,且A的阳离子的氧化性比B的阳离子的氧化性弱,C的阴离子所带的负电荷比D的阴离子所带的负电荷多,则它们的原子半径由大至小的顺序是( )
| A. | D>C>B>A | B. | A>B>C>D | C. | B>A>C>D | D. | A>B>D>C |
11.实验室制取下列气体,只能用排水法收集的是( )
| A. | Cl2 | B. | S02 | C. | NH3 | D. | NO |
8.下列说法中,正确的是( )
| A. | SO2能使FeCl3、KMnO4溶液迅速褪色 | |
| B. | 可以用澄清石灰水来鉴别SO2与CO2 | |
| C. | 硫粉在过量的纯氧中燃烧可以生成SO3 | |
| D. | 冷的浓硫酸和浓硝酸可以用铁桶装 |
15.除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
| 选项 | 含杂质的物质 | 试剂 | 除杂方法 |
| A | C2H4(SO2) | NaOH溶液 | 洗气 |
| B | C6H6(Br2) | Fe粉 | 蒸馏 |
| C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
| D | C2H6(C2H4) | 酸性KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
12.下列化学用语中,正确的是( )
| A. | Mg原子结构示意图  | B. | NaCl的电子式  | ||
| C. | CO2分子的结构式O-C-O | D. | 乙烯的结构简式CH2CH2 |

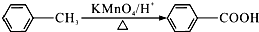
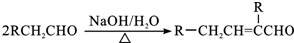
 .
.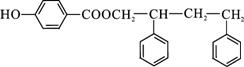 .
.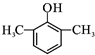 或
或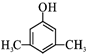 (写出其中一种的结构简式).
(写出其中一种的结构简式).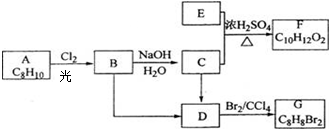
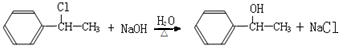
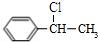 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$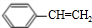 +NaCl+H2O
+NaCl+H2O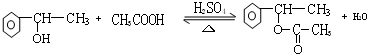
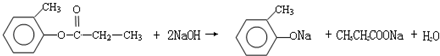 .
. .
.