题目内容
15.除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )| 选项 | 含杂质的物质 | 试剂 | 除杂方法 |
| A | C2H4(SO2) | NaOH溶液 | 洗气 |
| B | C6H6(Br2) | Fe粉 | 蒸馏 |
| C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
| D | C2H6(C2H4) | 酸性KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化硫与NaOH溶液反应,而乙烯不能;
B.溴、苯在Fe作催化剂条件下反应;
C.硝酸与NaOH溶液反应,而硝基苯不能;
D.乙烯被氧化生成二氧化碳气体.
解答 解:A.二氧化硫与NaOH溶液反应,而乙烯不能,则利用洗气法可除杂,故A正确;
B.溴、苯在Fe作催化剂条件下反应,不能除杂,应加NaOH溶液分液来除杂,故B错误;
C.硝酸与NaOH溶液反应,而硝基苯不能,则加NaOH溶液分液可除杂,故C正确;
D.乙烯被氧化生成二氧化碳气体引入新杂质,应用溴水除杂,故D错误;
故选BD.
点评 本题考查混合物分离提纯方法的选择和应用,为高频考点,把握物质的性质及性质的差异为解答的关键,侧重混合物分离方法及除杂的考查,注意除杂的原则,题目难度不大.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
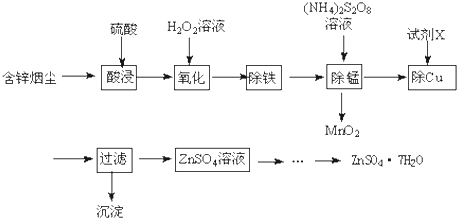
5.将“废杂铜烟尘”用硫酸吸收浸取,既可保护环境又可得到用途广泛的高纯硫酸锌.已知烟尘中主要含ZnO,还有少量的FeO、Fe2O3、CuO、MnO.制备工艺流程如图:
(1)硫酸锌溶液滴入石蕊试液,溶液变红,其原因是Zn2+水解使溶液显酸性,Zn2++2H2O?Zn(OH)2+2H+.
(2)H2O2氧化Fe2+的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)“除铁”时,溶液的pH应调整到3.2~5.2(相关金属离子生成氢氧化物沉淀的pH及沉淀完全的pH,金属离子开始沉淀时的浓度为1mol•L-1).
(4)“除锰”时溶液中发生反应的化学方程式为MnSO4+(NH4)2S2O8+2H2O=MnO2↓+(NH4)2SO4+2H2SO4或MnSO4+(NH4)2S2O8+2H2O=MnO2↓+2NH4HSO4+H2SO4.
(5)试剂X为Zn粉.
(6)由ZnSO4溶液需经过:蒸发浓缩、冷却结晶、过滤及干燥得ZnSO4•7H2O.
(1)硫酸锌溶液滴入石蕊试液,溶液变红,其原因是Zn2+水解使溶液显酸性,Zn2++2H2O?Zn(OH)2+2H+.
(2)H2O2氧化Fe2+的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)“除铁”时,溶液的pH应调整到3.2~5.2(相关金属离子生成氢氧化物沉淀的pH及沉淀完全的pH,金属离子开始沉淀时的浓度为1mol•L-1).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.5 | 8.0 |
| Cu2+ | 5.2 | 6.7 |
| Fe2+ | 5.8 | 8.8 |
(5)试剂X为Zn粉.
(6)由ZnSO4溶液需经过:蒸发浓缩、冷却结晶、过滤及干燥得ZnSO4•7H2O.

6.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式以下用于研究有机物的方法错误的是( )
| A. | 蒸馏常用于分离提纯液态有机混合物 | |
| B. | 燃烧法是确定有机物成分的有效方法之一 | |
| C. | 红外光谱通常用于分析有机物的相对分子质量 | |
| D. | 核磁共振氢谱的研究有助于确定有机物分子中氢原子的类型和数目比 |
10.现有部分元素的性质与原子(或分子)结构如表:
(1)写出元素T的原子结构示意图 .
.
(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是cd(填序号).
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式: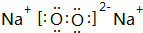 .
.
(4)元素T和氢元素以原子个数比1:1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:N2H4+2H2O2═N2↑+4H2O.
(5)T、W(+4价)、Y形成的正盐溶液中含有溶质0.20mol,另一溶液是200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是B
A.2.0mol/L B.1.5mol/L C.0.18mol/L D.0.24mol/L.
| 元素编号 | 元素性质与原子(或分子)结构 | |
| T | 最外层电子数是次外层电子数的3倍 | |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 | |
| Y | M层比K层少1个电子 | |
| Z | 第三周期元素的简单离子中半径最小 | |
| W | W带两个负电荷的阴离子与Ar具有相同电子层结构 | |
 .
.(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是cd(填序号).
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式:
 .
.(4)元素T和氢元素以原子个数比1:1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:N2H4+2H2O2═N2↑+4H2O.
(5)T、W(+4价)、Y形成的正盐溶液中含有溶质0.20mol,另一溶液是200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是B
A.2.0mol/L B.1.5mol/L C.0.18mol/L D.0.24mol/L.
20.下列实验中,现象及得出的结论正确的是( )
| 实 验 | 现 象 | 结论 | |
| A | 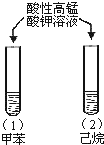 | 试管(1)中紫色褪去, 试管(2)中紫色未褪 | 苯环使甲基的活性增强 |
| B | 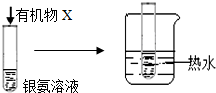 | 试管内壁有 银镜生成 | 有机物X中一定含有醛基 |
| C | 向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜悬浊液并加热 | 未见砖红色沉淀 | 淀粉未水解 |
| D | 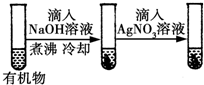 | 最后一只试管中有浅黄色沉淀 | 有机物中含有溴原子 |
| A. | A | B. | B | C. | C | D. | D |
5.在蒸发皿中用酒精灯加热蒸干下列物质的溶液然后灼烧,可以得到该物质固体的是( )
| A. | AlCl3 | B. | Na2SO3 | C. | KMnO4 | D. | MgSO4 |
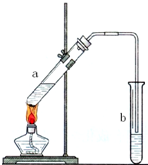 可用图示装置制取少量乙酸乙酯.已知乙酸乙酯的沸点低于乙醇.请填空:
可用图示装置制取少量乙酸乙酯.已知乙酸乙酯的沸点低于乙醇.请填空: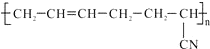 ,其具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
,其具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )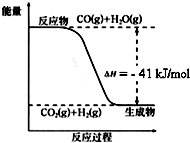 已知工业制氢气的反应为CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中能量变化如图所示.在500℃时的平衡常数 K=9.若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1mol/L,10min时达到平衡状态.
已知工业制氢气的反应为CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中能量变化如图所示.在500℃时的平衡常数 K=9.若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1mol/L,10min时达到平衡状态.