题目内容
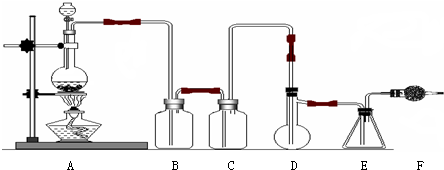
3.登山运动员常利用氢化钙固体作为能源提供剂.某兴趣小组用纯净干燥的氢气和金属钙制取氢化钙,所选装置图如下: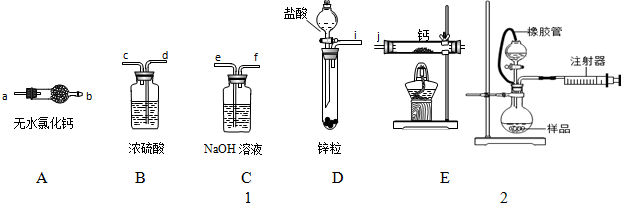
查阅资料:①钙易与水反应生成碱和气体.
②氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气.
(1)请按气流方向连接顺序i接e,f接d,c接j,k接 a
(填仪器接口的字母编号).
(2)装置A的作用是防止空气中的水蒸气进入E装置;装置C的作用是除去氢气中混有的氯化氢气体.
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞,②①④③(请按正确的顺序填入下列步骤的序号).
①加热反应一段时间 ②收集气体并检验其纯度
③关闭分液漏斗活塞 ④停止加热,充分冷却
(4)甲同学设计一个实验,测定上述实验中得到的氢化钙的纯度.请完善下列实验步骤.
①样品称量 ②加入足量的Na2CO3溶液(填化学式),搅拌、过滤 ③洗涤、干燥(填操作名称) ④称量碳酸钙的质量
(5)乙同学利用图2装置测定上述实验中得到的氢化钙的纯度.他称取46mg 所制得的氢化钙样品,记录开始时注射器活栓停留在10.00mL刻度处,反应结束后充分冷却,活栓最终停留在57.04mL刻度处.(上述气体体积均在标准状况下测定)
试通过计算求样品中氢化钙的纯度:91.3%.(计算结果保留一位小数)
分析 从装置可以看出,由装置D反应生成氢气,而生成的H2中混有HCl和H2O,故要先用C装置除去HCl,然后用B装置除去水蒸汽,即可得纯净干燥的氢气,通入E中与金属钙在加热条件下生成CaH2,由于金属钙能和水反应,故装置E的右端要连接装置A,防止空气中的水蒸气进入装置E,据此分析.
(1)一般制备纯净干燥的气体的实验装置的顺序为:制备装置→除杂装置→干燥装置等;
(2)钙能和水反应生成氢氧化钙和氢气;生成的氢气中混有HCl气体;
(3)实验过程中要保证整个装置内已充满氢气,实验的操作程序是:检查装置的气密性→产生氢气→收集氢气并进行验纯→加热反应→停止加热→继续通氢气至冷却→停止通入氢气;
(4)从最终称量碳酸钙可知,应加入碳酸盐溶液,使CaH2反应的同时得到碳酸钙沉淀,然后经过滤、洗涤、烘干、称量,确定纯度;
(5)由注射器D开始时活塞停留在10mL刻度处,反应结束后充分冷却,活塞最终停留57.04mL刻度处,可知生成氢气:57.04mL-10mL=47.04mL,所以氢气的质量为:$\frac{0.04704L}{22.4L/mol}$×2g/mol=0.0042g=4.2mg,设混合物中氢化钙的质量为x,生成氢气质量为y,则钙的质量为46mg-x,钙与水反应生成氢气质量为4.2mg-y,根据方程式CaH2+2H2O═Ca(OH)2+2H2↑、Ca+2H2O═Ca(OH)2+H2↑,列方程计算x、y的值,再根据质量分数定义计算;
解答 解:(1)钙属于极活泼的金属,极易与水反应生成氢氧化钙和氢气,而制备的氢气中会混有水蒸气和氯化氢,所以在与钙化合之前需要除杂和干燥,分别选用试剂是氢氧化钠和浓硫酸;同时为防止空气中水蒸气进入,最后还需要连接干燥管,所以正确的顺序为:i→e,f→d,c→j,k(或k,j)→a;
故答案为:i→e,f→d,c→j,k(或k,j)→a;
(2)由于钙能和水反应生成氢氧化钙和氢气,故在装置E的右端要连接装置A,防止空气中的水蒸气进入装置E;生成的氢气中混有HCl气体,通过装置C中的NaOH溶液的作用是除去氢气中的HCl,故答案为:防止空气中的水蒸气进入E装置;除去氢气中混有的氯化氢气体;
(3)由于多余的氢气需要燃烧反应掉,所以应该先收集一部分气体并检验其纯度,反应结束后还需要使氢化钙在氢气的氛围中冷却,所以应该最后关闭分液漏斗活塞,因此正确的顺序为②①④③,故答案为:②①④③;
(4)从最终称量碳酸钙可知,应加入碳酸钠溶液,使CaH2反应的同时得到碳酸钙沉淀,然后经过滤、洗涤、烘干、称量,确定纯度,
故答案为:Na2CO3;洗涤、烘干;
(5)由注射器D开始时活塞停留在10mL刻度处,反应结束后充分冷却,活塞最终停留57.04mL刻度处,可知生成氢气:57.04mL-10mL=47.04mL,所以氢气的质量为:$\frac{0.04704L}{22.4L/mol}$×2g/mol=0.0042g=4.2mg,设混合物中氢化钙的质量为x,生成氢气质量为y,则钙的质量为46mg-x,钙与水反应生成氢气质量为4.2mg-y,则:
CaH2+2H2O═Ca(OH)2+2H2↑
42 4
X Y
所以42:4=x:y,整理的y=$\frac{2x}{21}$
Ca+2H2O═Ca(OH)2+H2↑
40 2
46mg-x 4.2mg-y
所以40:2=(46mg-x):(4.2mg-y),将y=$\frac{2x}{21}$代入,解得x=42mg,所以样品中氢化钙的纯度为:$\frac{42mg}{46mg}$×100%=91.30%,
故答案为:91.3%
点评 本题以氢化钙制备为载体,考查实验基本技能与操作、对好题中的信息的利用、对实验装置的理解分析、物质分离提纯、化学计算、实验方案设计等,本题测重基本实验操作能力考查,是对学生综合能力的考查,难度中等.

| A. | 投入铁片产生H2的溶液中可大量存在H+,Mg2+,SO${\;}_{4}^{2-}$,NO${\;}_{3}^{-}$ | |
| B. | 可用稀硝酸除去试管内壁上的银镜 | |
| C. | 1.0mol•L-1的KNO3溶液中可大量存在H+,Fe2+,Cl-,SO${\;}_{4}^{2-}$ | |
| D. | 硫化铜溶于硝酸的离子方程式为CuS+2H+═H2S↑+Cu2+ |
| A. | 反应速率v(B)=0.13 mol•L-1•min-1 | B. | 该反应方程式中,x=1 | ||
| C. | 4min时,A的物质的量为0.75mol | D. | 4min时,A的转化率为50% |
| A. | 原子晶体中,共价键的键能越大,熔沸点越高 | |
| B. | 分子晶体中,分子间作用力越大,该分子越稳定 | |
| C. | 金属阳离子只能与阴离子构成晶体 | |
| D. | 正四面体构型的分子中,键角一定为109°28′ |
 Fe(OH)3+3H+,过量盐酸抑制FeCl3水解(结合离子方程式简要说明).
Fe(OH)3+3H+,过量盐酸抑制FeCl3水解(结合离子方程式简要说明).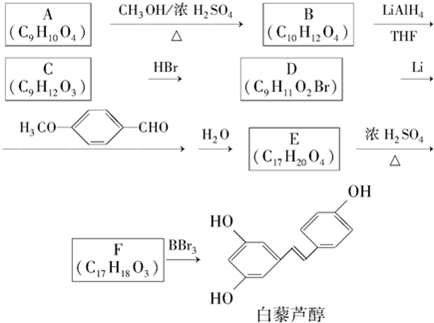
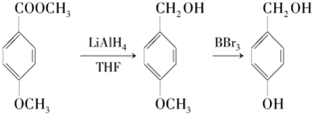
 .
.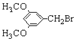 E
E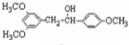 .
.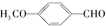 有多种同分异构体,写出符合下列条件的同分异构体的结构简式:
有多种同分异构体,写出符合下列条件的同分异构体的结构简式: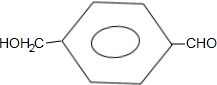 .
.