题目内容
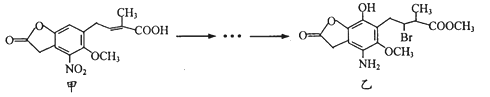
【题目】实验室以海绵铜(主要成分为Cu和CuO)为原料制取CuCl的主要流程如图所示。

已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60~70℃,原因是____________________。
(2)写出“转化”过程中的离子方程式____________________。
(3)“过滤Ⅱ”所得滤液经__________、__________、过滤等操作获得(NH4)2SO4晶体,可用作化学肥料。“过滤Ⅱ”所得滤渣主要成分为CuCl,用乙醇洗涤的优点是________________。
(4)氯化铵用量[![]() ]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是__________。
]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是__________。

(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:__________。(实验中可选试剂:0.1 mol·L1盐酸、10 mol·L1盐酸、蒸馏水、无水乙醇)
【答案】温度低溶解速度慢、温度过高铵盐分解 2Cu2++ SO32-+2Cl+H2O![]() 2CuCl↓+ SO42-+2H+ 蒸发浓缩 降温结晶 CuCl在乙醇中溶解度小且乙醇挥发快,避免CuCl被空气中O2氧化 生成的氯化亚铜又溶解于氯化铵溶液中 向产品中加入10 mol·L1盐酸,不断搅拌,至固体不再溶解,过滤,向滤液中加蒸馏水至大量固体析出,过滤,再用无水乙醇洗涤2~3次,干燥
2CuCl↓+ SO42-+2H+ 蒸发浓缩 降温结晶 CuCl在乙醇中溶解度小且乙醇挥发快,避免CuCl被空气中O2氧化 生成的氯化亚铜又溶解于氯化铵溶液中 向产品中加入10 mol·L1盐酸,不断搅拌,至固体不再溶解,过滤,向滤液中加蒸馏水至大量固体析出,过滤,再用无水乙醇洗涤2~3次,干燥
【解析】
实验流程中,海绵铜(主要成分为Cu和CuO)中加入硝酸铵和硫酸,酸性条件下硝酸根离子具有氧化性,可氧化海绵铜生成Cu2+,滤液中含有Cu2+、NH4+、H+、SO42-、NO3-,过滤后在滤液中加入亚硫酸铵,发生氧化还原反应生成CuCl,发生反应:2Cu2++SO32-+2Cl+H2O![]() 2CuCl↓+ SO42-+2H+,得到产品CuCl,据此分析。
2CuCl↓+ SO42-+2H+,得到产品CuCl,据此分析。
(1)物质“溶解氧化”时,既要考虑反应速率,还要考虑是否有副反应发生,温度低溶解速度慢、温度过高铵盐分解。答案为:温度低溶解速度慢、温度过高铵盐分解;
(2)“转化”中氧化产物为硫酸铵,滤液主要是硫酸铵。可知亚硫酸铵被溶液中的CuSO4氧化成硫酸铵,Cu2+被还原生成CuCl。答案为:2Cu2++SO32-+2Cl+H2O![]() 2CuCl↓+ SO42-+2H+;
2CuCl↓+ SO42-+2H+;
(3)“过滤Ⅱ”所得滤液为硫酸铵溶液,获取晶体需通过蒸发浓缩、降温结晶、过滤等操作。CuCl在乙醇中溶解度小且乙醇沸点低,易挥发,避免因水洗干燥时间长而导致CuCl被氧气氧化。答案为:蒸发浓缩、降温结晶;CuCl在乙醇中溶解度小且乙醇挥发快,避免CuCl被空气中O2氧化;
(4)根据题中已知条件,CuCl可溶于氯离子浓度较大的溶液中。当氯化铵用量增加到一定程度后,氯化亚铜的沉淀率减小,原因是生成的氯化亚铜又溶解于氯化铵溶液中。答案为:生成的氯化亚铜又溶解于氯化铵溶液中;
(5)由题目已知资料可知,CuCl难溶于水和乙醇,可溶于氯离子浓度较大的溶液中。若CuCl产品中混有少量CaSO4,向产品中加入10 mol·L1盐酸,不断搅拌,至固体不再溶解,过滤,向滤液中加蒸馏水至大量固体析出,过滤,再用无水乙醇洗涤2~3次,干燥即可得到纯净氯化亚铜。答案为:向产品中加入10 mol·L1盐酸,不断搅拌,至固体不再溶解,过滤,向滤液中加蒸馏水至大量固体析出,过滤,再用无水乙醇洗涤2~3次,干燥。

【题目】在三个体积均为2 L恒容密闭容器中,反应CO(g)+2H2(g)![]() CH3OH(g) ΔH<0达到平衡,得到如下数据。下列说法正确的是
CH3OH(g) ΔH<0达到平衡,得到如下数据。下列说法正确的是
容器编号 | 温度/K | 物质的起始物质的量/mol | 物质的平衡物质的量/mol | ||
CO(g) | H2(g) | CH3OH(g) | CH3OH(g) | ||
Ⅰ | T1 | 0.40 | 0.80 | 0 | 0.24 |
Ⅱ | T2 | 0 | 0 | 0.40 | 0.20 |
Ⅲ | T2 | a | b | ||
A.反应温度:T1<T2
B.达平衡时,转化率:α(CO,Ⅰ)+α(CH3OH,Ⅱ)>1
C.在容器Ⅲ中,若平衡时,CO的转化率大于H2,则![]()
D.在容器Ⅲ中,若起始时加入0.4 mol CO、0.4 mol H2和0.4 mol CH3OH,则此时v(正)>v(逆)
【题目】三氯化氮(NCl3)是一种消毒剂,可利用氯气与氯化铵溶液反应来制备。已知:三氯化氮的相关性质如下:
物理性质 | 化学性质 |
黄色油状液体,熔点为-40℃,沸点为 71℃,不溶于冷水、易溶于有机溶剂,密度为 1.65 gcm-3 | 95℃时爆炸,热水中发生水解 |
某小组同学选择下列装置(或仪器)设计实验制备三氯化氮并探究其性质:
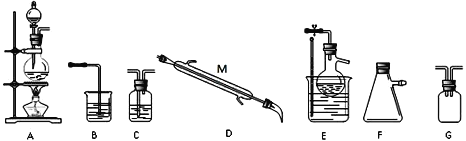
(1)NCl3的电子式为__________________;仪器 M 的名称是______________;
(2)如果气流的方向从左至右,装置连接顺序为A、G、_____________、B。(注明:F仪器使用单孔橡胶塞)
(3)C中试剂是_________________;B装置的作用是________________;
(4)写出E装置中发生反应的化学方程式_______________________________________
(5)当E装置的烧瓶中出现较多油状液体时停止反应。控制水浴加热温度为__________;
(6)已知三氯化氮不具有漂白性,三氯化氮与热水反应的化学方程式为NCl3+4H2O=NH3H2O+3HClO,请设计实验证明该水解反应的产物______________