题目内容
【题目】下列离子检验的方法正确的是
A.某溶液中加入KSCN溶液呈红色,说明原溶液不含有Fe2+离子
B.某溶液中通入氯气,然后再加入KSCN溶液呈红色,说明原溶液中一定有Fe2+离子
C.某溶液中加入氢氧化钠溶液生成红褐色沉淀,说明原溶液中一定有Fe3+离子
D.某溶液中加入稀硫酸溶液产生无色气体,说明原溶液中一定有![]() 离子
离子
【答案】C
【解析】
A.KSCN可以与Fe3+反应,而Fe2+与KSCN溶液不反应,如果该溶液既含Fe3+又含Fe2+,滴加KSCN溶液,溶液呈红色,证明存在Fe3+而不能证明没有Fe2+,A错误;
B.通入Cl2,氯气可以将Fe2+氧化成Fe3+,如果该溶液只含Fe3+,通入氯气后滴加KSCN溶液后也显红色,无法证明原溶液是否一定含有Fe2+,B错误;
C.加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+,C正确;
D.加入稀硫酸溶液产生无色气体,若有![]() ,也能产生无色气体,不能说明原溶液中一定有
,也能产生无色气体,不能说明原溶液中一定有![]() 离子,D错误;
离子,D错误;
故选C。

 名校课堂系列答案
名校课堂系列答案【题目】乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心。回答下列问题:
(1)乙烷可通过热裂解和氧化裂解制取乙烯。已知下列键能数据:
化学键 | C—C | C=C | C—H | H—H |
键能/ kJ·mol -1 | 347. 7 | 615 | 413. 4 | 436. 0 |
①乙烷直接裂解制乙烯的热化学方程式为_____________________________。
②氧化裂解制乙烯的热化学方程式为C2H6(g) + ![]() O2(g) = C2H4(g) + H2O(g) △H = - 105 kJ·mol-1 . 结合①分析,氧化裂解相对热裂解生产乙烯的优点是:_____________________________________(列举1点)。
O2(g) = C2H4(g) + H2O(g) △H = - 105 kJ·mol-1 . 结合①分析,氧化裂解相对热裂解生产乙烯的优点是:_____________________________________(列举1点)。
(2)利用生物乙醇在某种分子筛催化下可脱水制取乙烯,相应反应如下:
I. C2H5OH(g) ![]() C2H4(g) + H2O(g)
C2H4(g) + H2O(g)
Ⅱ. 2C2H5OH(g) ![]() (C2H5)2O(g) + H2O(g)
(C2H5)2O(g) + H2O(g)
平衡常数[Kp是用平衡分压代替平衡浓度(平衡分压=总压×物质的量分数)]及产品选择性如下图所示:
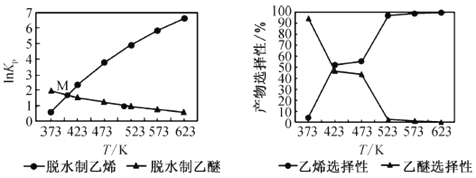
①反应 C2H5OH(g) ![]() C2H4(g) + H2O(g) 的△H______(填“>”或“<”)0。
C2H4(g) + H2O(g) 的△H______(填“>”或“<”)0。
②关于上图中交点M,下列说法正确的是________(填字母)。
a. 一段时间内,反应I、Ⅱ的速率相等
b. 某温度下,反应I、Ⅱ的平衡常数相等
c. 一段时间内,反应I、Ⅱ中乙醇的转化率相等
(3)利用煤制合成气,再由合成气间接制乙烯包含的反应有:
I. CO(g) +2H2(g) ![]() CH3OH(g) △H=a kJ·mol-1
CH3OH(g) △H=a kJ·mol-1
Ⅱ. 2CH3QH(g) ![]() C2H4(g) + 2H2O(g) △H =b kJ·mol-1
C2H4(g) + 2H2O(g) △H =b kJ·mol-1
①反应 2CO(g) + 4H2(g) ![]() C2H4(g) + 2H2O(g) △H = _________kJ·mol-1 (用 a、b表示)。
C2H4(g) + 2H2O(g) △H = _________kJ·mol-1 (用 a、b表示)。
②在容积为1 L的密闭容器中,投入2 mol CO和4 mol H2,10 min后,测得c(CO) = 1. 2 mol·L-1·min-1,则10 min内v(H2)=_____________ mol·L-1·min-1。