题目内容
【题目】表是元素周期表的一部分,表中的每个字母表示一种短周期元素,回答下列问题: 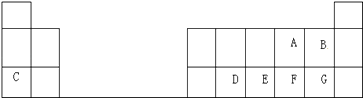
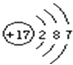
(1)画出G的原子结构示意图
(2)A,B,E,F五种元素的原子半径最大的是(填化学式).
(3)E,F,G元素的最高价氧化物对应水化物的酸性最强的是:(用化学式表示).
(4)A,B,G的氢化物最稳定的是(用化学式表示).
(5)写出C和B形成化合物的电子式 .
【答案】
(1)
(2)P
(3)HClO4
(4)HF
(5)![]()
【解析】解:由元素在周期表中的位置可知A为O元素,B为F元素,C为Na元素,D为Si元素,E为P元素,F为S元素,G为Cl元素,(1)G为Cl,原子核外有3个电子层,最外层电子数为7,原子结构示意图为  ,所以答案是:
,所以答案是:  ;(2)一般来说,原子核外电子层数越多,原子半径越大,同周期元素从左到右原子半径逐渐减小,则A、B、E、F五种元素的原子半径最大为E,即P,所以答案是:P;(3)非金属性P<S<Cl,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越大,则酸性最强的为HClO4 , 所以答案是:HClO4;(4)非金属性F>O>Cl,元素的非金属性越强,对应的氢化物越稳定,HF的稳定性最强,所以答案是:HF;(5)C和B形成化合物为NaF,为离子化合物,电子式为
;(2)一般来说,原子核外电子层数越多,原子半径越大,同周期元素从左到右原子半径逐渐减小,则A、B、E、F五种元素的原子半径最大为E,即P,所以答案是:P;(3)非金属性P<S<Cl,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越大,则酸性最强的为HClO4 , 所以答案是:HClO4;(4)非金属性F>O>Cl,元素的非金属性越强,对应的氢化物越稳定,HF的稳定性最强,所以答案是:HF;(5)C和B形成化合物为NaF,为离子化合物,电子式为 ![]() ,所以答案是:
,所以答案是: ![]() .
.

练习册系列答案
相关题目