题目内容
已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A.该溶液的pH=4 |
| B.升高温度,溶液的pH增大 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
B
解析

练习册系列答案
相关题目
常温下,有关下列4种溶液的说法正确的是
| ① | ② | ③ | ④ |
| 0.1 mol·L-1氨水 | pH=11氨水 | 0.1 mol·L-1盐酸 | pH=3盐酸 |
A.由水电离出的c(H+):③>①
B.①稀释到原来的100倍,pH与②相同
C.①与③混合,若溶液pH=7,则溶液中c(NH4+)>c(Cl-)
D.②与④等体积混合,混合液pH>7
为了同时对农作物施用含有N、P、K三种元素的化肥,对于给定的化肥:①KCl②K2CO3 ③Ca(H2PO4)2④NH4Cl⑤CO(NH2)2,不适合的组合是
| A.②③④ | B.①③④ | C.①③⑤ | D.①③④⑤ |
下表是相同温度下三种酸的一些数据,下列判断正确的是
A.在相同温度下, > > > > |
B.室温时,若在NaZ溶液中加水,则 / / · · 的比值变小,若加少量盐酸,则比值变大 的比值变小,若加少量盐酸,则比值变大 |
C.等物质的量浓度的NaX、NaY和NaZ的混合溶液,则 < < < < |
D.在相同温度,从HX的数据可以说明:弱电解质溶液浓度越低,电离度越大,且 > > > > =0.01 =0.01 |
某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是( )
A.含有大量S 的溶液中肯定不存在Ag+ 的溶液中肯定不存在Ag+ |
| B.0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀 |
| C.Ag2SO4的溶度积常数(Ksp)为1×10-3 |
| D.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。医院抢救钡离子中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。
已知:Ksp(BaCO3)=5.1×10-9;Ksp(BaSO4)=1.1×10-10
下列推断正确的是( )
| A.不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4) |
| B.抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替 |
| C.若误饮c(Ba2+)=1.0×10-5 mol/L的溶液时,会引起钡离子中毒 |
| D.可以用0.36 mol/L的Na2SO4溶液给钡离子中毒患者洗胃 |
①pH=2的CH3COOH溶液;
②pH=2的盐酸;
③pH=12的氨水;
④pH=12的NaOH溶液。
相同条件下,有关上述溶液的比较中,正确的是( )
| A.水电离的c(H+):①=②=③=④ |
| B.将②、③溶液混合后,pH=7,消耗溶液的体积:②<③ |
| C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D.向溶液中加入100 mL水后,溶液的pH:③>④>①>② |
将浓度为0.1 mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A.c(H+) | B.Ka(HF) | C.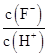 | D.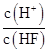 |
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图,下列判断正确的是( )
| A.a、c两点溶液的导电能力相同 |
| B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-) |
| C.用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc |
| D.a、b、c三点溶液水的电离程度a>b>c |