题目内容
16.下列反应既是氧化还原反应,又是吸热反应的是( )| A. | 锌粒与稀H2SO4的反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 灼热的炭与CO2的反应 | D. | 浓硫酸的稀释 |
分析 有元素化合价变化的反应为氧化还原反应;常见的吸热反应有Ba(OH)2•8H2O与NH4Cl反应、C参加的氧化还原反应、大多数的分解反应等,以此来解答.
解答 解:A.锌粒与稀H2SO4的反应为放热反应,故A不选;
B.Ba(OH)2•8H2O与NH4Cl的反应为吸热反应,但不是氧化还原反应,故B不选;
C.C元素化合价发生变化,属于氧化还原反应,也为吸热反应,故C选;
D.浓硫酸的稀释放热,但属于物理变化,故D不选.
故选C.
点评 本题考查氧化还原反应和吸热反应,为高考常见题型,注意把握反应中的变化及能量变化为解答的关键,侧重学生归纳整合能力的考查,题目难度不大.

练习册系列答案
相关题目
4.下列物质发生变化时,所克服的粒子间相互作用属同种类型的是( )
| A. | 氯化铵与乙醇分别受热变为气体 | B. | 氯化钠与氯化氢分别溶解在水中 | ||
| C. | 碘与干冰分别受热变为气体 | D. | NaHSO4受热熔化与溶于水变为溶液 |
11.一定温度下在容积恒定的密闭容器中,进行反应A(s)+2B(g)?C(g)+D(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( )
①混合气体的密度
②容器内气体的压强
③混合气体总物质的量
④B物质的量浓度.
①混合气体的密度
②容器内气体的压强
③混合气体总物质的量
④B物质的量浓度.
| A. | ①④ | B. | 只有②③ | C. | ②③④ | D. | 只有④ |
1.元素周期律和元素周期表是学习化学的重要工具,下列说法不正确的是( )
| A. | 第1列中的碱金属和第17列元素的单质熔、沸点变化趋势相同 | |
| B. | 元素周期表中从ⅢB族到ⅡB族十个纵列的元素都是金属元素 | |
| C. | 在整个18列元素中,第14列元素形成的化合物种类最多 | |
| D. | 在整个18列元素中,第3列元素种类最多 |
7.①制备纳米TiO2的方法之一是TiCl4水解生成TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.
②用NaOH测定滤液的浓度:准确称量1.000gNaOH固体质量,配制成250mL溶液,准确量取25.00mL溶液装在锥形瓶,滴加2滴酚酞作指示剂.把滤液装在酸式滴定管中,调节液面排除气泡后,滤液的凹液面刚好在“0”刻度,滴定NaOH溶液,达到终点记录读数.实验重复3次.记录见下表.
(1)TiCl4水解生成TiO2•xH2O的化学方程式为TiCl4+(x+2)H2O=TiO2•xH2O↓+4HCl
(2)配制成250mL溶液使用的量具是250mL容量瓶;
(3)滴定终点的现象是浅红色溶液变为无色,半分钟内不变色.
(4)滤液中溶质的物质的量浓度为0.125mol•L-1.
(5)若在滴定终点读取滴定管刻度时,俯视标准液液面,使对测定结果偏高. (填“偏高”、“偏低”或“无影响”)
②用NaOH测定滤液的浓度:准确称量1.000gNaOH固体质量,配制成250mL溶液,准确量取25.00mL溶液装在锥形瓶,滴加2滴酚酞作指示剂.把滤液装在酸式滴定管中,调节液面排除气泡后,滤液的凹液面刚好在“0”刻度,滴定NaOH溶液,达到终点记录读数.实验重复3次.记录见下表.
| 滴定次数 | NaOH溶液体积/mL | 滴定消耗滤液体积/mL |
| 1 | 25.00 | 20.02 |
| 2 | 25.00 | 17.10 |
| 3 | 25.00 | 19.98 |
(2)配制成250mL溶液使用的量具是250mL容量瓶;
(3)滴定终点的现象是浅红色溶液变为无色,半分钟内不变色.
(4)滤液中溶质的物质的量浓度为0.125mol•L-1.
(5)若在滴定终点读取滴定管刻度时,俯视标准液液面,使对测定结果偏高. (填“偏高”、“偏低”或“无影响”)
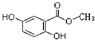 所示.
所示.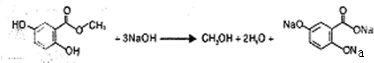 .(不用写反应条件)
.(不用写反应条件) .
.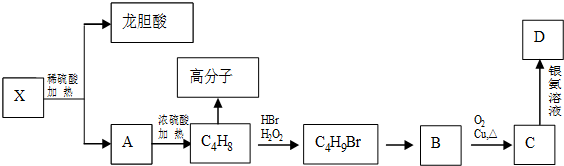
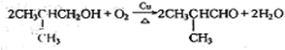 ,它的反应类型是氧化反应反应.
,它的反应类型是氧化反应反应.
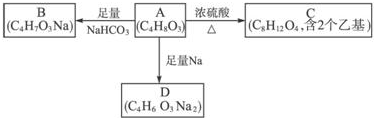
 .
.
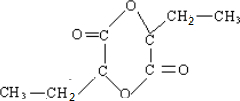 .
.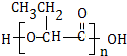 .
.