题目内容
11.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 0.1 mol•L-1Mg(NO3)2溶液中含有0.2 NA个NO3- | |
| B. | 标准状况下,11.2LH2O含有的分子数为0.5NA | |
| C. | 3mol Cu和足量稀硝酸反应产生2 NA个NO分子 | |
| D. | 1 mol Cl2与足量NaOH溶液反应,转移电子数为NA |
分析 A、溶液体积不明确;
B、标况下,水为液态;
C、根据得失电子数守恒来计算;
D、氯气与氢氧化钠的反应为歧化反应.
解答 解:A、溶液体积不明确,故溶液中的硝酸根的个数无法计算,故A错误;
B、标况下,水为液态,不能根据气体摩尔体积来计算其物质的量,故B错误;
C、根据电子守恒计算,3molCu失6mole-,HNO3还原为NO,生成NO的物质的量n=$\frac{6}{3}$=2mol,即产生2NA个NO分子,故C正确;
D、氯气与氢氧化钠的反应为歧化反应,1mol氯气转移1mol电子,即NA个,故D正确.
故选CD.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
1.配制250mL 0.10mol/L的NaOH溶液时,下列实验操作会使配得的溶液中NaOH物质的量浓度偏大的是( )
| A. | 转移溶液后未洗涤烧杯和玻璃棒就直接定容 | |
| B. | 称量时,在天平托盘上放上称量纸,将NaOH固体放在纸上称量 | |
| C. | 在容量瓶中进行定容时俯视刻度线 | |
| D. | 定容后把容量瓶倒置摇匀,发现液面低于刻度线,又补足了所缺的水 |
2.下列各项表述与示意图一致的是( )
| A. | 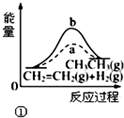 图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)+△Q,0<△Q;使用和未使用催化剂时,反应过程中的能量变化 | |
| B. | 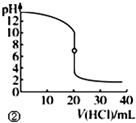 图②表示25℃时,用0.01mol•L-1盐酸滴定一定体积的0.01mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. | 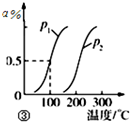 图③表示CH4(g)+H2O(g)?CO(g)+3H2(g)+△Q,反应CH4的转化率与温度、压强的关系,且p1>p2、0<△Q | |
| D. | 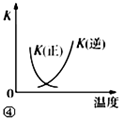 图④中曲线表示反应2SO2(g)+O2(g)?2SO3(g)+△Q,0<△Q;正、逆反应的平衡常数K随温度的变化 |
16.实验室保存下列试剂的方法有错误的是( )
| A. | 新制氯气盛放在棕色试剂瓶中,存放于低温避光的地方 | |
| B. | 固体碘常盛放在棕色细口瓶中 | |
| C. | 液溴易挥发,盛放在用水液封的棕色试剂瓶中 | |
| D. | 金属钠易被氧化,少量金属钠应储存在煤油中 |
3.NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温下18g 铝放入足量浓硫酸中转移电子数2NA | |
| B. | 0.1mol•L-1的稀硫酸中含有H+个数为0.2NA | |
| C. | 常温常压下48g的O3中含有氧原子数为3NA | |
| D. | 1.8g NH4+中含有的电子数为0.1NA |
20.下列叙述中正确的是( )
| A. | 一定温度下,向AgCl的饱和溶液中加入NaCl晶体,Ksp(AgCl)增大 | |
| B. | NH4Cl溶液中存在:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 向CH3COOH溶液中加入少量CH3COONa固体,溶液pH增大 | |
| D. | 某温度下,KW=1×10-12,则pH=11的氨水中,c(OH-)=1×10-8mol/L |
1.下列关于化学反应速率的叙述不正确的是( )
| A. | 食物放在冰箱中会减慢变质的速率 | |
| B. | 实验室制备CO2时,可通过增加石灰石的用量来加快反应速率 | |
| C. | 制取乙酸乙酯时加入浓硫酸作催化剂可加快酯化反应的速率 | |
| D. | 实验室制取H2时,常用锌粒代替锌粉以降低反应的速率 |
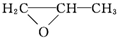 +H2O→
+H2O→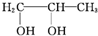 .
.
 .
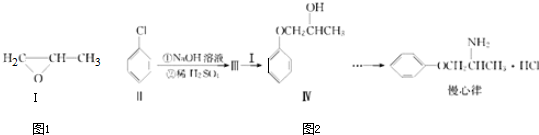
.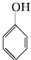 +3Br2→
+3Br2→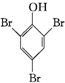 ↓+3HBr.
↓+3HBr.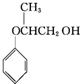 .
.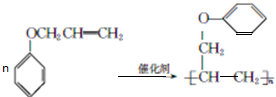 .
. 如图是NO2与CO发生可逆反应过程中的能量变化示意图,请回答下列问题.
如图是NO2与CO发生可逆反应过程中的能量变化示意图,请回答下列问题.