题目内容
13.将过氧化钠投入FeCl2溶液中,可观察到的实验现象是( )| A. | 有绿色气体产生 | B. | 没有沉淀生成 | ||
| C. | 有白色沉淀生成 | D. | 有红褐色沉淀生成 |
分析 Na2O2投入FeCl2溶液反应中Na2O2和水反应,生成的氢氧化钠和氧气,氢氧化钠再与氯化亚铁反应生成氢氧化亚铁,氢氧化亚铁被氧化为氢氧化铁.
解答 解:将Na2O2投入FeCl2溶液中,发生的反应为:2Na2O2+2H2O=4NaOH+O2↑,2NaOH+FeCl2=Fe(OH)2↓+2NaCl,4Fe(OH)2+O2+H2O=4Fe(OH)3,4Fe(OH)2是白色沉淀易被氧化为红褐色的Fe(OH)3沉淀,所以看到的现象是:有大量气泡生成,和红褐色沉淀生成.
故选:D.
点评 本题考查的是钠化合物的性质、氢氧化钠的性质,正确分析反应过程是解本题的关键,题目难度不大.

练习册系列答案
相关题目
9.关于SO2的下列叙述中,正确的是( )
| A. | SO2在有的反应中显示氧化性,有的反应中显示还原性 | |
| B. | SO2是酸性氧化物,溶于水生成稳定的亚硫酸 | |
| C. | SO2气体通入Na0H溶液中一定得到Na2SO3 | |
| D. | SO2气体通入BaCl2溶液中,能生成白色沉淀 |
1.Ⅰ.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,X和Y两物质的浓度随时间变化情况如图1.
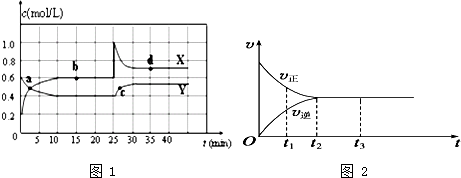
(1)该反应的化学方程式为 (反应物或生成物用符号X、Y表示):Y?2X.
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是b、d.
Ⅱ.(3)如图2是可逆反应X2+3Y2?2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是BD
A.t1时,只有正方向反应 B.t2时,反应达到限度
C.t2~t3,反应不再发生 D.t2~t3,各物质的浓度不再发生变化
Ⅲ.以下是关于化学反应2SO2+O2?2SO3的两个素材:
素材1:某温度和压强下,2升容器中,不同时间点测得密闭体系中三种物质的物质的量
素材2:反应在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数,SO2的转化率越大,化学反应的限度越大)
根据以上的两个素材回答问题:
(4)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应平均速率为0.0075 mol•L-1•s-1.
(5)根据素材2中分析得到,提高该化学反应限度的途径有增大压强或在一定范围内降低温度.
(6)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应条件是温度为600℃,压强为1MPa.

(1)该反应的化学方程式为 (反应物或生成物用符号X、Y表示):Y?2X.
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是b、d.
Ⅱ.(3)如图2是可逆反应X2+3Y2?2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是BD
A.t1时,只有正方向反应 B.t2时,反应达到限度
C.t2~t3,反应不再发生 D.t2~t3,各物质的浓度不再发生变化
Ⅲ.以下是关于化学反应2SO2+O2?2SO3的两个素材:
素材1:某温度和压强下,2升容器中,不同时间点测得密闭体系中三种物质的物质的量
| 时间(s)物质的量(mol)物质 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| SO2 | 1 | 0.7 | 0.5 | 0.35 | 0.2 | 0.1 | 0.1 | 0.1 |
| O2 | 0.5 | 0.35 | 0.25 | 0.18 | 0.1 | 0.05 | 0.05 | 0.05 |
| SO3 | 0 | 0.3 | 0.5 | 0.65 | 0.8 | 0.9 | 0.9 | 0.9 |
| 压强转化率温度 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600℃ | 73.7 | 85.8 | 90.0 | 96.4 |
(4)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应平均速率为0.0075 mol•L-1•s-1.
(5)根据素材2中分析得到,提高该化学反应限度的途径有增大压强或在一定范围内降低温度.
(6)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应条件是温度为600℃,压强为1MPa.
8.下列混合物分离与提纯的方法中不正确的是( )
| A. | CO2中混有HCl,将混合气体通入饱和的NaHCO3溶液中 | |
| B. | 从溴水中提取溴,用酒精萃取分液 | |
| C. | 用蒸馏的方法从酒精溶液中提取酒精 | |
| D. | 从较稀的KNO3溶液中得到KNO3晶体,可先对溶液进行蒸发浓缩、冷却结晶,再过滤 |
18.氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
(1)根据如图1能量变化示意图,请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如表:
①该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$
②试判断K1>K2(填写“>”,“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
④在某一时间段中反应速率与反应过程的曲线关系如图2,则图中氨的百分含量最低的时间段是D
A.t0-t1 B.t2-t3 C.t3-t4 D.t5-t6
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图3所示,下列说法正确的是CD.
a.A、C两点的反应速率:A>C
b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C
d.由状态B到状态A,可以用加热的方法
(4)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的$\frac{7}{8}$,则N2的转化率a(N2)=25%,以NH3表示该过程的反应速率v(NH3)=0.075mol/(L.min).
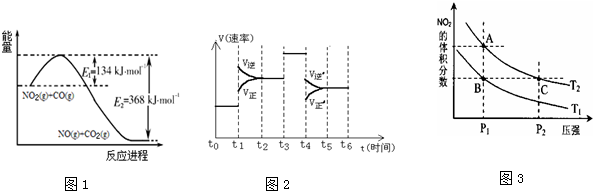
(1)根据如图1能量变化示意图,请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②试判断K1>K2(填写“>”,“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
④在某一时间段中反应速率与反应过程的曲线关系如图2,则图中氨的百分含量最低的时间段是D
A.t0-t1 B.t2-t3 C.t3-t4 D.t5-t6
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图3所示,下列说法正确的是CD.
a.A、C两点的反应速率:A>C
b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C
d.由状态B到状态A,可以用加热的方法
(4)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的$\frac{7}{8}$,则N2的转化率a(N2)=25%,以NH3表示该过程的反应速率v(NH3)=0.075mol/(L.min).

5.现有下列短周期元素性质的有关数据:
(1)根据元素周期律确定a至h 8种元素在周期表中的位置,将它们的元素编号填入下表相应的空格内.
(2)上述元素形成的氢化物中,分子间存在氢键的有(填氢化物的化学式)HF、NH3.
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛.在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH).
①氢化铝锂易水解,最初得三种产物,请写出其水解反应方程式LiAlH4+4H2O=LiOH+Al(OH)3+4H2↑.
②与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请写出这种还原剂的电子式.写出该物质受热分解的反应方程式:2NaBH4$\frac{\underline{\;\;△\;\;}}{\;}$2B+2NaH+3H2↑.
(4)原子数相同,电子总数相同的分子或离子互称等电子体.在元素周期表中,与碳相邻的两种元素可形成具有石墨型晶体结构的“白石墨”,“白石墨”和石墨具有等电子体特征,写出“白石墨”的最小结构单元-六元环的结构式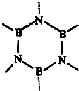 .
.
| 元素符号 | a | b | c | d | e | f | g | h |
| 原子半径/mm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合计 | +1 | -1 | -3 | +3 | -2 | +3 | +1 | +1 |
| 族/周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | ||||||||
| 3 |
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛.在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH).
①氢化铝锂易水解,最初得三种产物,请写出其水解反应方程式LiAlH4+4H2O=LiOH+Al(OH)3+4H2↑.
②与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请写出这种还原剂的电子式.写出该物质受热分解的反应方程式:2NaBH4$\frac{\underline{\;\;△\;\;}}{\;}$2B+2NaH+3H2↑.
(4)原子数相同,电子总数相同的分子或离子互称等电子体.在元素周期表中,与碳相邻的两种元素可形成具有石墨型晶体结构的“白石墨”,“白石墨”和石墨具有等电子体特征,写出“白石墨”的最小结构单元-六元环的结构式
 .
.
2.下列有关化学用语表述正确的是( )
| A. | S2-的结构示意图: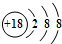 | |
| B. | CO2的比例模型: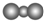 | |
| C. | 邻羟基苯甲酸的结构简式: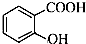 | |
| D. | 质子数为79、中子数为118的金(Au)原子:${\;}_{79}^{118}$Au |