题目内容
2.下列有关化学用语表述正确的是( )| A. | S2-的结构示意图: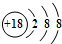 | |
| B. | CO2的比例模型: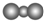 | |
| C. | 邻羟基苯甲酸的结构简式: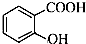 | |
| D. | 质子数为79、中子数为118的金(Au)原子:${\;}_{79}^{118}$Au |
分析 A.硫离子的核电荷数为16,不是18;
B.二氧化碳分子中,碳原子的相对体积大于O原子;
C.邻羟基苯甲酸中,羟基和羧基在苯环的邻位碳上;
D.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数.
解答 解:A.S为16号元素,核外有16个电子,得到两个电子形成S2-,则S2-的结构示意图: ,故A错误;
,故A错误;
B.二氧化碳分子中,碳原子的原子半径大于氧原子,其正确的比例模型为: ,故B错误;
,故B错误;
C.邻羟基苯甲酸相当于羟基取代了苯甲酸中羧基邻位H形成的,其结构简式为: ,故C正确;
,故C正确;
D.质子数为79、中子数为118的金(Au)原子的质量数为197,该原子正确的表示方法为:79197Au,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,涉及比例模型、结构简式、离子结构示意图、元素符号等知识,明确常见化学用语的概念及书写原则为解答关键.

练习册系列答案
相关题目
13.将过氧化钠投入FeCl2溶液中,可观察到的实验现象是( )
| A. | 有绿色气体产生 | B. | 没有沉淀生成 | ||
| C. | 有白色沉淀生成 | D. | 有红褐色沉淀生成 |
10.小明为研究添加食品中的食盐中的碘酸钾的稳定性,查阅文献得到相关信息如下,回答下列问题
(1)相同温度下,pH=0时,碘酸钾最不稳定.
(2)pH=7时,随着温度的升高碘酸钾的稳定性减弱.(填“增强”,“不变”或“减弱”);
(3)小明猜想,碘酸钾因转化为碘单质.请设计一个实验方案证明是否有碘单质生成:取样,加淀粉溶液,如溶液变蓝说明有碘生成,反之,没碘生成.
| 编号 | 碘酸钾浓度/mol/L | pH | 碘酸钾损失率/% | |||
| 30℃ | 50℃ | 80℃ | 100℃ | |||
| 1 | 0.003 | 0 | 21 | 70.3 | 71 | 77.3 |
| 2 | 0.003 | 7 | 0 | 0.3 | 0.67 | 1 |
| 3 | 0.003 | 14 | 1.3 | 2.7 | 1.3 | 1 |
(2)pH=7时,随着温度的升高碘酸钾的稳定性减弱.(填“增强”,“不变”或“减弱”);
(3)小明猜想,碘酸钾因转化为碘单质.请设计一个实验方案证明是否有碘单质生成:取样,加淀粉溶液,如溶液变蓝说明有碘生成,反之,没碘生成.
17.下列方程式书写正确的是( )
| A. | 苏打溶液中加入过量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 用硫酸酸化的橙色的重铬酸钾(K2Cr2O7)溶液与乙醇作用生成乙酸和草绿色三价铬,可以用于检测是否酒后驾驶:2Cr2O72-+3C2H5OH+16H+→4Cr3++3CH3COOH+11H2O | |
| C. | 用铜为电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 表示乙醇燃烧热的热化学方程式(△H的绝对值正确):C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0kJ•mol-1 |
7.下列实验事实陈述正确并且有因果关系的是( )
| A. | 滴加BaC12溶液生成白色沉淀 原溶液中有SO42- | |
| B. | 用洁净铂丝蘸取溶液进行焰色反应:火焰呈黄色 原溶液中有Na+无K+ | |
| C. | 滴加氯水和CC14,振荡、静置.下层溶液显紫色 原溶液中有I- | |
| D. | 滴加几滴稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝 原溶液中无NH4+ |
11.向明矾溶液中加入Ba(OH)2 溶液,当SO42- 恰好沉淀完全时,这时铝元素的存在形式是( )
| A. | Al(OH)3 沉淀 | B. | 只有AlO2-离子 | ||
| C. | Al(OH)3 沉淀和Al3+ | D. | Al(OH)3 沉淀 和AlO2-离子 |
12.下列说法中正确的是( )
| A. | 标准状况下,18g水的体积为22.4L | |
| B. | 1mol H2的质量只有在标准状况下才约为2g | |
| C. | 1mol H2和O2的混合气体的体积约为22.4L | |
| D. | 标准状况下,a L氧气和氮气的混合物含有的分子数约为$\frac{a}{22.4}$ NA个 |
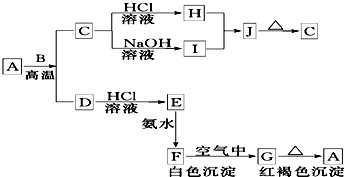 A是一种红棕色金属氧化物,B、D是金属单质,C也是一种金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体,受热后容易发生分解.
A是一种红棕色金属氧化物,B、D是金属单质,C也是一种金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体,受热后容易发生分解.