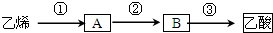
题目内容
(1)标明下面反应中电子转移的方向和数目,并指出还原剂.
2Na+Cl2
2NaCl ,还原剂是 .
(2)Na2CO3的俗名 .
(3)Na2O2与水反应的离子方程式为 .
2Na+Cl2
| ||
(2)Na2CO3的俗名
(3)Na2O2与水反应的离子方程式为
考点:氧化还原反应,钠的重要化合物
专题:氧化还原反应专题,元素及其化合物
分析:(1)Na元素失去电子,为还原剂,该反应中转移2e-,以此标明反应中电子转移的方向和数目;
(2)Na2CO3为纯碱,也称为苏打;
(3)Na2O2与水反应生成NaOH和氧气.
(2)Na2CO3为纯碱,也称为苏打;
(3)Na2O2与水反应生成NaOH和氧气.
解答:
解:(1)Na元素失去电子,为还原剂,该反应中转移2e-,则反应中电子转移的方向和数目为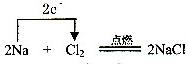 ,
,
故答案为: ;Na;
;Na;
(2)Na2CO3为纯碱,也称为苏打,故答案为:纯碱(或苏打);
(3)Na2O2与水反应生成NaOH和氧气,离子反应为2Na2O2+2H2O═4Na++4OH-+O2↑,故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑.
 ,
,故答案为:
 ;Na;
;Na;(2)Na2CO3为纯碱,也称为苏打,故答案为:纯碱(或苏打);
(3)Na2O2与水反应生成NaOH和氧气,离子反应为2Na2O2+2H2O═4Na++4OH-+O2↑,故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑.
点评:本题考查较综合,涉及氧化还原反应、离子反应及钠的化合物,注重高频考点的考查,把握反应中元素的化合价变化及离子反应中保留化学式的物质即可解答,题目难度不大.

练习册系列答案
相关题目
下列有关实验的做法正确的是( )
| A、分液时,分液漏斗中的上层液体应由下口倒出 |
| B、用加热分解的方法不能区分碳酸钠和碳酸氢钠两种固体 |
| C、配制0.1000mol?L-1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流 |
| D、检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 |
下列离子在pH=2的溶液中能大量共存的是( )
| A、Na+、Ba2+、SO42- |
| B、K+、Cl-、CO32- |
| C、Al3+、NO3-、SO42- |
| D、Fe3+、OH-、NO3- |
下列说法正确的是( )
| A、浓硫酸溶于水的过程属于放热反应 |
| B、既有化学键断裂又有化学键生成的过程一定属于化学反应 |
| C、物质导电的过程一定是物理变化 |
| D、同分异构体之间的相互转化一定是化学变化 |