题目内容
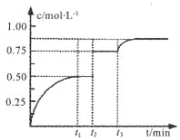
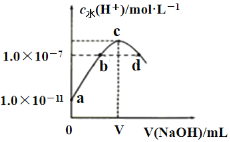
【题目】常温下,在新制氯水中滴加NaOH溶液,溶液中水电离的![]() 与NaOH溶液体积之间的关系如下图所示,下列推断正确的是( )
与NaOH溶液体积之间的关系如下图所示,下列推断正确的是( )
A. 用pH试纸测定a点对应溶液,其![]()
B. b、d点对应的溶液中都存在:![]()
C. c点对应的溶液中:![]()
D. 常温下加水稀释d点对应的溶液,溶液的pH增大
【答案】C
【解析】
A.a点新制氯水溶液,溶液显酸性,由水电离出的c水(H+)=10-11mo/L,溶液中OH-完全是由水电离出来的,所以c(OH-)=c水(H+)=10-11mo/L,则溶液中c(H+)=![]() =10-3mol/L,则溶液pH=3,但新制氯水有漂白性,不能用pH试纸测量其pH,应该用pH计,故A错误;
=10-3mol/L,则溶液pH=3,但新制氯水有漂白性,不能用pH试纸测量其pH,应该用pH计,故A错误;
B.d点对应溶液中溶质为NaCl、NaClO和NaOH,根据电荷守恒可知:c(Na+)+c(H+)=c(OH-)+c(Cl-)+c(ClO-),此时溶液为碱性,则c(OH-)>c(H+),所以c(Na+)>c(Cl-)+c(ClO-),故B错误;
C.c点,氯水与氢氧化钠溶液恰好完全反应生成等物质的量的NaCl、NaClO,溶液呈碱性,ClO-水解,新制氯水中起始时含等量的HCl和HClO,所以有c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+),故C正确;
D.加水稀释d点对应的溶液,d点为碱性溶液,加水稀释时促使溶液的碱性减弱,所以pH值降低,故D错误;
答案选C。

【题目】在1L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.10 | 0.09 |
② | 800 | 0.20 | 0.20 | 0.10 |
③ | 800 | 0.20 | 0. 30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法错误的是
A. 实验①中,若5min时测得n(M) =0.05mol,则0至5min时间内,用N表示的平均反应速率v(N) =0.01 mol/( L·min)
B. 实验②中,该反应的平衡常数K= 1.0
C. 实验③中,达到平衡时,X的转化率为60%
D. 实验④中,达到平衡时,b>0.06