题目内容
【题目】用0.2000 mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000 mol/L的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“ 0”或“0”刻度线稍下,并记下读数;④量取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴甲基橙溶液;⑤用标准液滴定至终点,记下滴定管液面读数。⑥重复以上滴定操作2-3次。请回答:
(1)以上步骤有错误的是(填编号)____________________
(2)步骤④中,量取20.00 mL待测液应使用_________________(填仪器名称)
(3)步骤⑤滴定时眼睛应注视______________________________;判断到达滴定终点的依据是:______________________________________。
(4)以下是实验数据记录表
滴定 次数 | 盐酸体积 (mL) | NaOH溶液体积读数(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.00 | 18.10 |
2 | 20.00 | 0.00 | 16.20 |
3 | 20.00 | 0.00 | 16.16 |
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是__________
A. 锥形瓶装液前,留有少量蒸馏水 B. 滴定结束时,仰视读数
C.滴定前滴定管尖嘴无气泡,滴定结束有气泡 D.锥形瓶用待测液润洗
E. NaOH标准液保存时间过长,有部分变质
(5)根据表中记录数据,通过计算可得,该盐酸浓度为: ____________mol/L
【答案】① 酸式滴定管 锥形瓶内颜色变化 当滴入最后一滴时,溶液由红色变橙色,且半分钟内颜色不变 B D 0.1618
【解析】
(1)滴定管用蒸馏水洗涤后还要用待装的溶液润洗,以防止滴定管内壁上的水膜稀释溶液,引起实验误差。
(2)中和滴定是精确度较高的定量实验,与此相匹配的仪器是滴定管,还要注意溶液的酸碱性以选择对应的滴定管。
(3)中和滴定的关键之一就是要准确判断滴定终点,因此操作时眼睛始终注视锥形瓶内溶液颜色的变化;因为滴定前盐酸中滴入了甲基橙,溶液为红色,根据恰好中和时溶液pH突跃,滴定终点时溶液由红色变为橙色,且半分钟内颜色不变。
(4)表中第1次实验滴定结束时消耗NaOH溶液体积明显偏大,分析选项时,一看是否是读数造成的误差,滴定管的0刻度在上,越往下数值越大;二看是否是HCl的物质的量造成的误差,根据NaOH+HCl=NaCl+H2O反应,NaOH与HCl以等物质的量反应; 三看NaOH变质生成Na2CO3,等物质的量的NaOH和Na2CO3消耗HCl的物质的量有无变化。
(5)根据表中消耗的NaOH溶液的数据先判断数据的有效性,然后计算出消耗NaOH溶液的平均体积,最后计算出待测液盐酸的浓度。
(1)碱式滴定管用蒸馏水洗涤后还要用0.2000mol/LNaOH溶液润洗,防止NaOH溶液被滴定管内壁上的水膜稀释,引起实验误差,故有错误的编号是①。
(2)中和滴定是精确度较高的定量实验,与此相匹配的仪器是滴定管,所以步骤④中,量取20.00 mL待测液(盐酸)应使用酸式滴定管。
(3)中和滴定的关键之一就是要准确判断滴定终点,所以操作时眼睛始终注视锥形瓶内溶液颜色变化;待测的盐酸中事先加入了甲基橙,溶液显红色,根据恰好中和时溶液pH突跃,滴定终点时溶液显橙色,所以判断到达滴定终点的依据是:当滴入最后一滴时,溶液由红色变橙色,且半分钟内颜色不变。
(4)表中第1次滴定记录的NaOH溶液体积明显偏大,A.锥形瓶装液前,留有少量蒸馏水,HCl的物质的量没有变化,故消耗NaOH溶液的体积不受影响,A项错误;B.滴定管的0刻度在上,越往下数值越大,读数应从上往下读,仰视读数会使NaOH溶液体积偏大,B项正确;C. 滴定前滴定管尖嘴无气泡,滴定结束有气泡,滴定管液面上升,使NaOH溶液体积偏小, C项错误;D.锥形瓶用待测液润洗,HCl的物质的量增大,消耗的NaOH溶液体积偏大,D项正确;E.NaOH标准液保存时间过长,有部分NaOH变质生成Na2CO3,以甲基橙作指示剂时滴定过程有反应Na2CO3+2HCl=2NaCl+CO2↑+H2O,1molNaOH~0.5molNa2CO3~1molHCl,所以滴定消耗NaOH溶液体积不受影响,E项错误;答案选BD。
(5)表中第1次实验数据误差太大舍去,取第2、3次实验数据,消耗标准NaOH溶液体积的平均值=![]() =16.18mL,该盐酸浓度为
=16.18mL,该盐酸浓度为![]() 。
。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案【题目】某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
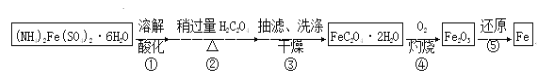
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。
请回答:
(1)下列操作或描述正确的是________。
A.步骤②,H2C2O4稍过量主要是为了抑制Fe2+水解
B.步骤③,采用热水洗涤可提高除杂效果
C.步骤③,母液中的溶质主要是(NH4)2SO4和H2C2O4
D.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(2)如图装置,经过一系列操作完成步骤③中的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):

开抽气泵→a→b→d→________→c→关抽气泵。
a.转移固液混合物;b.关活塞A;c.开活塞A;d.确认抽干;e.加洗涤剂洗涤
抽滤和普通过滤相比,优点是___________________________________________。
(3) 称取一定量的FeC2O4·2H2O试样,用硫酸溶解,
采用KMnO4滴定法测定,折算结果如下:
n(Fe2+)/mol | n( | 试样中FeC2O4·2H2O的质量分数 |
9.80×10ˉ4 | 9.80×10ˉ4 | 0.980 |
由表中数据推测试样中最主要的杂质是____________________。
(4)实现步骤④必须用到的两种仪器是____________________
(供选仪器:a.烧杯;b.坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶);
该步骤的化学方程式是______________________________________。
(5)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是________________________________。