题目内容
有机化学中常用18O原子作示踪原子来研究乙酸与乙醇反应生成酯的反应机理,反应过程中酸分子断裂C—O单键,醇分子断裂O—H键。试述书写CH3COOH和CH3CH218OH反应的化学方程式:
已知反应: KClO3 + 6HCl =" KCl" + 3Cl2 + 3H2O ,若用K35ClO3与H37Cl作用,则所得氯气的相对分子质量为 .
已知反应: KClO3 + 6HCl =" KCl" + 3Cl2 + 3H2O ,若用K35ClO3与H37Cl作用,则所得氯气的相对分子质量为 .
CH3COOH+CH3CH218OH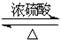 CH3CO18OCH2CH3+H2O;73.33
CH3CO18OCH2CH3+H2O;73.33
 CH3CO18OCH2CH3+H2O;73.33
CH3CO18OCH2CH3+H2O;73.33试题分析:在酯化反应中羧酸提供羟基,醇提供氢原子,所以该反应的方程式应该是CH3COOH+CH3CH218OH
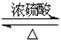 CH3CO18OCH2CH3+H2O;在反应KClO3 + 6HCl =" KCl" + 3Cl2 + 3H2O中氧化剂是氯酸钾、还原剂是氯化钾。其中氧化剂和还原剂的物质的量之比是1︰5,所以如果用K35ClO3与H37Cl作用,则所得氯气中35Cl与37Cl原子个数之比是1︰5,所以氯元素的平均相对原子质量是1/6×35+5/6×37=36.67,则该氯气分子的物质的量是36.67×2=73.33。
CH3CO18OCH2CH3+H2O;在反应KClO3 + 6HCl =" KCl" + 3Cl2 + 3H2O中氧化剂是氯酸钾、还原剂是氯化钾。其中氧化剂和还原剂的物质的量之比是1︰5,所以如果用K35ClO3与H37Cl作用,则所得氯气中35Cl与37Cl原子个数之比是1︰5,所以氯元素的平均相对原子质量是1/6×35+5/6×37=36.67,则该氯气分子的物质的量是36.67×2=73.33。点评:在氧化还原反应中,如果是同一种元素的高价态额低价态之间发生氧化还原反应,则产物的价态只能处于中间,且氧化产物的价态不高于还原产物的,据此可以判断还原产物和氧化产物。

练习册系列答案
相关题目
 2CO(g) ΔH2="+172.5" kJ/mol ②
2CO(g) ΔH2="+172.5" kJ/mol ② MnCl2+Cl2↑+2H2O中,氧化剂和还原剂物质的量之比为1∶2
MnCl2+Cl2↑+2H2O中,氧化剂和还原剂物质的量之比为1∶2