题目内容
在100mL FeI2溶液中缓缓通入标准状况下的氯气3.36L,反应完全后,溶液中有一半的Fe2+被氧化生成Fe3+。则原来FeI2溶液的物质的量浓度为( )
| A.1 mol·L-1 | B.1.2 mol·L-1 | C.1.5 mol·L-1 | D.6 mol·L-1 |
B
试题分析:氯气与FeI2溶液反应,先应该与碘离子反应,碘离子反应完后再与亚铁离子反应,所以溶液中有一半的Fe2+被氧化生成Fe3+,碘离子已经反应完全。离子方程式是2Fe2++8I-+5 Cl2=2Fe+4I2+10 Cl-,n(Cl2)=0.15mol,所以n(FeI2)=0.12mol,浓度是1.2mol·L-1
点评:本题要求学生的思维严密,离子的氧化性强弱要清楚,属于有一定难度的习题。

练习册系列答案
相关题目
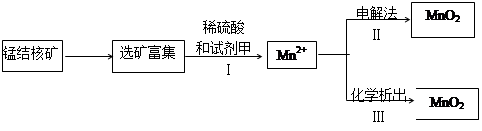
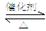 2SO3,在一密闭容器中一定时间内达到平衡.
2SO3,在一密闭容器中一定时间内达到平衡.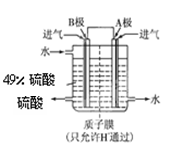
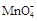 + —— Fe3++ Mn2++
+ —— Fe3++ Mn2++