��Ŀ����
����˵����ȷ����
A��MnO2��4HCl(Ũ) MnCl2��Cl2����2H2O�У��������ͻ�ԭ�����ʵ���֮��Ϊ1��2 MnCl2��Cl2����2H2O�У��������ͻ�ԭ�����ʵ���֮��Ϊ1��2 |
| B��2H2S��SO2��3S����2H2O�У���������ͻ�ԭ�������ʵ���֮��Ϊ1��1 |
C��3S��6KOH  2K2S��K2SO3��3H2O�У��������ͱ���ԭ����Ԫ������֮��Ϊ2��1 2K2S��K2SO3��3H2O�У��������ͱ���ԭ����Ԫ������֮��Ϊ2��1 |
| D��5NH4NO3��4N2��2HNO3��9H2O�У���Ӧ�з���������Ӧ�ͷ�����ԭ��Ӧ�ĵ�Ԫ������֮��Ϊ5��3 |
��AD
���������A��MnO2���ϼ۽�������������HCl���ϼ���������ԭ������4molHCl�μӷ�Ӧֻ��2mol������������A��ȷ��
B���ӷ�Ӧ��2molH2S����ԭ���������õ���������2molS��1molSO2������������ԭ�õ���ԭ����1molS������B����
C��3molS��Ӧ������2molS���ϼ۽��ͱ���ԭ������ԭ��Ӧ������1molS���ϼ����߱���������������Ӧ������C����
D����Ӧ��NH4+�е�N�ɩ�3������0�ۣ�����������Ӧ��NO3���е�N��+5�۽���0�ۣ�������ԭ��Ӧ������D��ȷ��
����������������ԭ��Ӧ�����жϼ���ؼ��㡣

��ϰ��ϵ�д�
 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д�
�����Ŀ
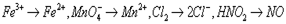 ��
��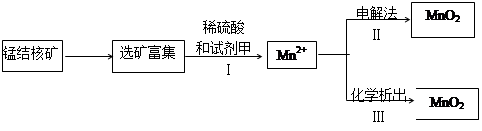
 MnCl2��Cl2����2H2O�У�������������������Ũ���ᷴӦ�Ƶ�3.55gCl2������
MnCl2��Cl2����2H2O�У�������������������Ũ���ᷴӦ�Ƶ�3.55gCl2������ MnCl2��Cl2����2H2O������4.35g�������̹�����������Ũ�����ַ�Ӧ��ת�Ƶ��ӵ����ʵ����뱻������HCl�����ʵ����ֱ�Ϊ
MnCl2��Cl2����2H2O������4.35g�������̹�����������Ũ�����ַ�Ӧ��ת�Ƶ��ӵ����ʵ����뱻������HCl�����ʵ����ֱ�Ϊ MnCl2 + Cl2�� + 2H2O
MnCl2 + Cl2�� + 2H2O