��Ŀ����
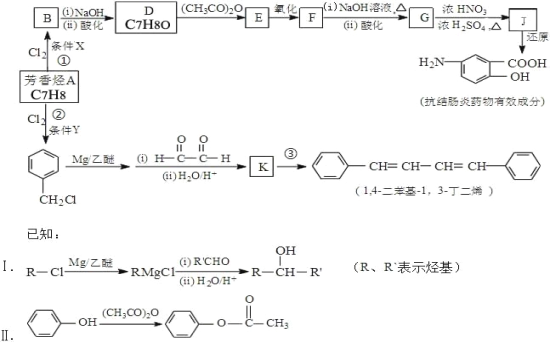
����Ŀ���л�����ԭ��1,4-������-1,3-����ϩ��ij���᳦��ҩ����Ч�ɷֵĺϳ�·�����£����ַ�Ӧ��ȥ�Լ�����������
��1�����᳦��ҩ����Ч�ɷַ����еĺ���������������________��
��2�����еķ�Ӧ������________��G����J�ķ�Ӧ������________��
��3���ٵĻ�ѧ����ʽ��________��
��4��F�Ľṹ��ʽ��________��
��5���۵Ļ�ѧ����ʽ��________��
��6�����D��E��F��G������Ӧ��Ŀ����________��
��7��1,4-������-1,3-����ϩ�ж���ͬ���칹�壬д��������������������ͬ���칹��Ľṹ��ʽ��_________��
a���ṹ����������������������״�ṹ b�������ϵ�һ����ȡ������������
���𰸡��ǻ� �Ȼ�����ȡ����Ӧ![]()

 �������ǻ�����ֹ���ǻ���������
�������ǻ�����ֹ���ǻ���������![]()
![]()
��������
��1�����ݿ��᳦��ҩ����Ч�ɷַ��ӽṹ��ʽ����֪�京���������������ǻ����Ȼ�����ȷ�����ǻ����Ȼ���
��2���ױ��IJ���±����������������ͬ�����ǹ��գ�G����J�ķ�Ӧ������Ũ���ᡢŨ���ᡢ���ȣ����Է�Ӧ������ȡ����Ӧ����ȷ�������գ� ȡ����Ӧ��
��3�����ݿ��᳦��ҩ����Ч�ɷַ��ӵĽṹ��ʽ�жϣ�DΪ�ڼױ��ӣ�����BΪ���ȼױ������Ļ�ѧ����ʽ��![]() ����ȷ����
����ȷ����![]() ��
��
��4��������֪����D��EӦ�DZ������ǻ��ķ�Ӧ��E��F�Ǽ��������ķ�Ӧ������F�Ľṹ��ʽΪ ����ȷ����
����ȷ���� ��
��
��5����1,4-������-1,3-����ϩ�ýṹ��ʽ����֪���ķ�Ӧ����ʽ�ж���������ȥ��Ӧ����ѧ����ʽ����
 ����ȷ����
����ȷ����
 ��
��
��6��D��E�ѷ��ǻ�ת��Ϊ������Ŀ���Ƿ�ֹE��F�����з��ǻ���������F��G�ְ�������ԭΪ���ǻ����������������DZ������ǻ�����ֹ���ǻ�������������ȷ�����������ǻ�����ֹ���ǻ�����������
��7��������ĿҪ��1,4-������-1,3-����ϩ��ͬ���칹���еı����ϵ�һ����ȡ�����������֣� 2����������ȡ����Ӧ��ȫ��ͬ����2�������ǶԳƽṹ�����Կ���1���������ɣ������ϵ�һ����ȡ�����������֣�˵��ÿ�������϶��ж�λȡ����������ͬ���칹��Ľṹ��ʽΪ![]()
![]() ����ȷ��
����ȷ��![]() ��
��![]() ��
��

 ��У����ϵ�д�
��У����ϵ�д�

