题目内容
氧元素与多种元素具有亲和力,所形成化合物的种类很多。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为________。氧元素与氟元素能形成OF2分子,该分子的空间构型为________。
(2)根据等电子原理,在NO2+离子中氮原子轨道杂化类型是________;1 mol O22+中含有的π键数目为________个。
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。Cr3+基态核外电子排布式为________。
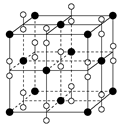
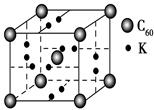
(4)钙在氧气中燃烧时得到一种钙的氧化物晶体,其晶体结构如图所示,则该钙的氧化物的化学式为________。
(5)下列物质的分子与O3分子的结构最相似的是________。
(6)O3分子是否为极性分子?________。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为________。氧元素与氟元素能形成OF2分子,该分子的空间构型为________。
(2)根据等电子原理,在NO2+离子中氮原子轨道杂化类型是________;1 mol O22+中含有的π键数目为________个。
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。Cr3+基态核外电子排布式为________。

(4)钙在氧气中燃烧时得到一种钙的氧化物晶体,其晶体结构如图所示,则该钙的氧化物的化学式为________。
(5)下列物质的分子与O3分子的结构最相似的是________。
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(1)F>N>O;V形 (2)sp;2NA
(3)1s22s22p63s23p63d3 (4)CaO2 (5)C (6)是
(3)1s22s22p63s23p63d3 (4)CaO2 (5)C (6)是
(1)由洪特规则的特例可知,氮元素的第一电离能大于氧元素(大于氮元素的“左邻右舍”),小于氟元素;由价层电子对互斥理论可知,OF2分子的空间构型是V形。(2)根据等电子原理,NO22+离子与CO2互为等电子体,两者的结构相似,NO2+离子中氮原子的杂化方式与CO2中碳原子的杂化方式相同,都是sp杂化;O22+与N2(其中有一个σ键和两个π键)互为等电子体,因此O22+中有2个π键。(4)钙在氧气中燃烧所得到的氧化物晶体中Ca2+与O22—的最简个数比为1:1。(5)(6)根据价层电子对互斥理论分析,SO2与O3分子的结构最相似,且都是极性分子。

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
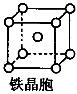
 3Na2O+2Fe+9N2↑。
3Na2O+2Fe+9N2↑。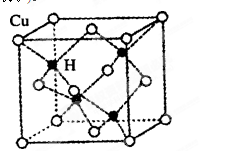

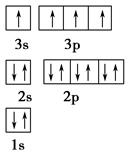
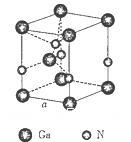
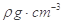 。列出计算氮化镓晶胞边长a的表达式:a=_______cm。
。列出计算氮化镓晶胞边长a的表达式:a=_______cm。