题目内容
9.下列情况一定能使反应速率加快的方法是( )①升温 ②改变反应物浓度 ③增加生成物浓度 ④加压.
| A. | ①②③ | B. | ①③ | C. | ②③ | D. | ①②③④ |
分析 ①升高温度反应速率加快;
②改变生成物浓度,不一定影响反应物的浓度;
③增加反应物浓度,反应速率加快;
④增大压强对有气体参加的反应,反应速率加快.
解答 解:①升高温度,增加单位体积内的活化分子数,有效碰撞增加,反应速率加快,故①正确;
②改变生成物浓度,不一定影响反应物的浓度的增大,反应速率不一定增大,故②错误;
③增加反应物浓度,单位体积内活化分子增大,有效碰撞增加,反应速率加快,故③正确;
④增大压强对有气体参加的反应,反应速率加快,若没有气体参加,压强对反应速率不影响,故④错误;
故选B.
点评 本题考查影响化学反应速率的常见因素,为高频考点,注意反应中固体、纯液体的量发生改变对反应速率无影响是学生在解题中容易忽略的知识,难度不大.

练习册系列答案
相关题目
17.某溶液中含有HCO3-、SO32-、CH3COO-、CO32-四种离子,若向其中加入Na2O2后,溶液中离子浓度基本保持不变的是( )
| A. | HCO3- | B. | SO32- | C. | CH3COO- | D. | CO32- |
4.实验室需用480mL0.10mol/L的硫酸铜溶液,以下操作正确的是( )
| A. | 将12.00g胆矾配成500mL溶液 | |
| B. | 将12.50g胆矾溶于少量水中,再用水稀释至500mL | |
| C. | 称取7.68g硫酸铜,加入500mL水 | |
| D. | 在80mL0.6mol/L CuSO4溶液中加入400mL水 |
14.研究表明:多种海产品如虾、蟹、牡蛎等,体内含有+5价的砷(As)元素,但它对人体是无毒的,砒霜的成分是As2O3,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜+大量维生素C=砒霜.下面有关解释不正确的是( )
| A. | 维生素C能将+5价砷氧化成As2O3 | |
| B. | 维生素C具有还原性 | |
| C. | 青菜中含有维生素C | |
| D. | 生成砒霜的过程中砷元素发生氧化反应 |
19.X、Y、Z、M、N代表五种金属.有以下化学反应:
①水溶液中:X+Y2+═X2++Y
②Z+2H2O(冷)═Z(OH)2+H2↑
③M、N为电极与N盐溶液组成原电池,发生的电极反应为:M-2e-═M2+
④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化,则这五种金属的活泼性由弱到强的顺序是( )
①水溶液中:X+Y2+═X2++Y
②Z+2H2O(冷)═Z(OH)2+H2↑
③M、N为电极与N盐溶液组成原电池,发生的电极反应为:M-2e-═M2+
④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化,则这五种金属的活泼性由弱到强的顺序是( )
| A. | M<N<Y<X<Z | B. | N<M<X<Y<Z | C. | N<M<Y<X<Z | D. | X<Z<N<M<Y |


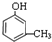
 ,
,
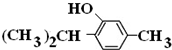 +3H2$→_{△}^{Ni}$
+3H2$→_{△}^{Ni}$
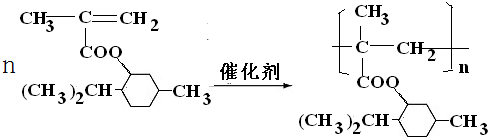 ;.
;.

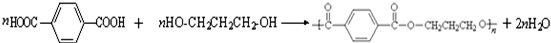 .
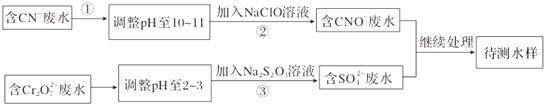
. ,请你设计出合理的反应流程图.
,请你设计出合理的反应流程图.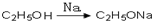 、
、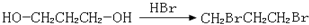 、
、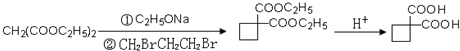 .
.