题目内容
14.常温下,下列各组离子在指定溶液中能大量共存的是( )| A. | pH=1的溶液中:Fe2+、NO3-、Cl-、Na+ | |
| B. | Na2S溶液中:SO42-、K+、Cl-、Cu2+ | |
| C. | c(H+)=1.0×10-13 mol•L-1溶液中:C6H5O-、K+、SO42-、Br- | |
| D. | 能使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、HCO3- |
分析 A.pH=1的溶液为酸性溶液,硝酸根离子在酸性条件下能够氧化亚铁离子;
B.铜离子与硫化钠反应生成硫化铜沉淀;
C.c(H+)=1.0×10-13 mol•L-1溶液为碱性溶液,溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
D.能使甲基橙呈红色的溶液为酸性溶液,溶液中存在大量氢离子,碳酸氢根离子酸性大于氢氧化铝,碳酸氢根离子与偏铝酸根离子反应生成氢氧化铝沉淀,且偏铝酸根离子与碳酸氢根离子都与氢离子反应.
解答 解:A.pH=1的溶液为酸性溶液,Fe2+、NO3-在酸性溶液中能够发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.Cu2+与Na2S反应生成CuS沉淀,在溶液中不能大量共存,故B错误;
C.c(H+)=1.0×10-13 mol•L-1溶液中存在大量氢氧根离子,C6H5O-、K+、SO42-、Br-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.能使甲基橙呈红色的溶液为酸性溶液,HCO3-酸性大于氢氧化铝,AlO2-、HCO3-之间反应生成氢氧化铝沉淀,且二者都都与酸性溶液中的氢离子反应,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
11.下列实验方案不合理的是( )
| A. | 用pH试纸测定氯水的pH | |
| B. | 用焰色反应鉴别NaCl和KNO3 | |
| C. | 用AgNO3溶液鉴别NO2和Br2蒸气 | |
| D. | 用饱和NaHCO3溶液除去CO2中混有的HCl杂质气体 |
2.化学与生产、生活息息相关,下列说法错误的是( )
| A. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 | |
| B. | 纤维素在人体内可以水解为葡萄糖,故可作人类的营养物质 | |
| C. | 用Na2S做沉淀剂,除去废水中的Cu2+和Hg2+ | |
| D. | “地沟油”禁止食用,但可以用来做肥皂 |
6.下列说法正确的是( )
| A. | 洗涤沉淀的操作是将沉淀置于滤纸上(已放置在漏斗中),边用玻璃棒搅拌边加蒸馏水冲洗 | |
| B. | 酸碱中和滴定常用的指示剂有酚酞、甲基橙和石蕊试液 | |
| C. | 除去Fe(OH)3胶体中的NaCl时,可将其装在用半透膜做的袋子里,放在流动的蒸馏水中,该分离方法称为渗析 | |
| D. | 将适量植物油、酒精和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可以制得肥皂 |
3.下列关于化学用语的表示正确的是( )
| A. | CO2的电子式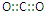 | |
| B. | CCl4的比例模型: | |
| C. | 含有18个中子的氯原子的核素符号:${\;}_{17}^{35}$Cl | |
| D. | 硫原子的结构示意图: |
4.下列关于常见化学物质的应用不正确的是( )
| A. | 过氧化钠能用作供氧剂 | |
| B. | 氯化钠可用作净水剂 | |
| C. | 味精可用作食品添加剂 | |
| D. | 小苏打是一种膨松剂,可用于制作馒头和面包 |
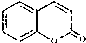 )是一种用途广泛的香料,其合成路线如图:
)是一种用途广泛的香料,其合成路线如图: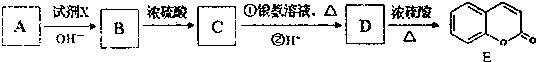
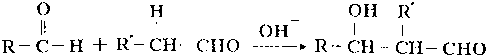
 ;
;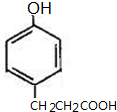 、
、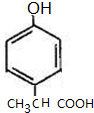 (写出一种即可).
(写出一种即可).