题目内容
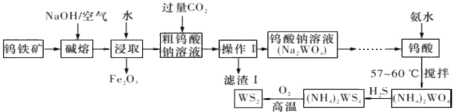
【题目】锌钡白是BaSO4和ZnS的混合物,ZnS难溶于水。某化工厂用重晶石为原料制备锌钡白,生产过程中会产生大量废气(主要成分为CO2、CO及少量SO2和硫蒸气等),为防止污染空气并提高原料利用率,生产中采用下述工艺流程:
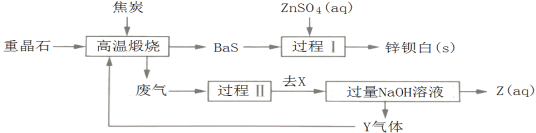
下列叙述错误的是
A.重晶石和钡餐的化学成分相同
B.Y气体的循环使用可以防止污染空气并能提高原料利用率
C.Z(aq)中的阴离子是OH-和CO32-
D.高温煅烧过程中焦炭的作用是为反应提供热量和作还原剂
【答案】C
【解析】
根据题中的工业流程可知,重晶石与碳发生氧化还原反应,重晶石被还原得硫化钡及废气,硫化钡与硫酸锌发生复分解反应可得硫酸钡和硫化锌即锌钡白,废气(主要成分为CO2、CO及少量SO2和硫蒸气等)经过过程Ⅱ得X,X应为S,去硫后的废气主要是CO2、CO及少量SO2,经过NaOH溶液,CO2、SO2被氢氧化钠吸收,则得到的Y为CO,CO再循环利用,还原重晶石,据此答题。
A.重晶石和钡餐的主要化学成分均为硫酸钡,故A正确;
B. Y(CO)气体的循环使用可以防止污染空气并能提高原料利用率,故B正确;
C. Z(aq)中的阴离子是OH-、CO32-和SO32-,故C错误;
D.焦炭的作用是燃烧生成CO为反应提供热量和作还原剂,故D正确;
答案选C。

练习册系列答案
 全能闯关100分系列答案
全能闯关100分系列答案
相关题目