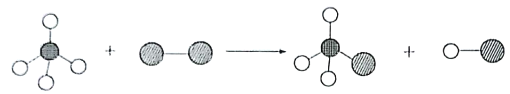
题目内容
【题目】某有机物0.3克完全燃烧后生成224毫升(标准状况)二氧化碳和0.18克水。已知该物质的蒸气对氢气的相对密度为30,试求:
(1)有机物的分子式___________
(2)试写出该有机物可能的结构简式并命名____________________。
【答案】C2H4O2 CH3COOH 乙酸 HCOOCH3 甲酸甲酯
【解析】
有机物的蒸气密度是相同条件下氢气的30倍,则其相对分子质量为30×2=60,根据原子守恒计算有机物分子中N(C)、N(H),再结合相对分子质量计算有机物分子中N(O),据此确定有机物分子式;根据分子式确定其可能的结构。
(1)有机物的蒸气密度是相同条件下氢气的30倍,则其相对分子质量为30×2=60,该有机物0.3g完全燃烧后,生成224mLCO2 (标准状况下)和0.18gH2O;0.3g有机物的物质的量=![]() =0.005mol,n(CO2)=
=0.005mol,n(CO2)= ![]() =0.01mol;0.18gH2O的物质的量为
=0.01mol;0.18gH2O的物质的量为![]() =0.01mol,根据原子守恒,可以知道有机物分子中N(C)=
=0.01mol,根据原子守恒,可以知道有机物分子中N(C)=![]() =2;N(H)=
=2;N(H)=![]() =4,则有机物分子中N(O)=
=4,则有机物分子中N(O)= ![]() =2,故有机物分子式为C2H4O2;
=2,故有机物分子式为C2H4O2;
答:该有机物分子式为C2H4O2;
(2)有机物分子式为C2H4O2,则该有机物的结构简式为CH3COOH,乙酸;HCOOCH3,甲酸甲酯;
答: 该有机物可能的结构简式及命名:CH3COOH,乙酸;HCOOCH3,甲酸甲酯。

【题目】某地环保部门将收集到的一定量酸雨试样分成甲、乙、丙、丁四份,进行如图所示的实验探究。
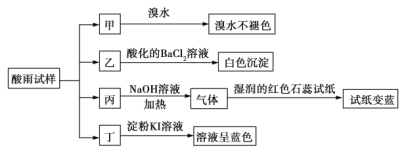
已知酸雨试样中可能含有下表所示的某些离子:
阳离子 |
|
阴离子 |
|
请回答下列问题:
(1)![]() 是______,
是______,![]() 是______。
是______。
(2)可能存在的阴离子是______,能证明该阴离子是否存在的简单实验操作为______。
(3)写出丁试样中滴加淀粉![]() 溶液所发生反应的离子方程式:______。
溶液所发生反应的离子方程式:______。
(4)某次降雨收集到![]() 雨水,向雨水中滴加
雨水,向雨水中滴加![]() 的
的![]() 溶液,充分反应后测得溶液中
溶液,充分反应后测得溶液中![]() ,再向该溶液中加入足量的
,再向该溶液中加入足量的![]() 溶液,经过滤、蒸干、称重,测得沉淀的质量为
溶液,经过滤、蒸干、称重,测得沉淀的质量为![]() 。假设雨水的酸性仅由
。假设雨水的酸性仅由![]() 和
和![]() 的排放所致,则排放到空气中的
的排放所致,则排放到空气中的![]() 和
和![]() 的物质的量之比约为______(不考虑
的物质的量之比约为______(不考虑![]() 的相互反应)。
的相互反应)。