题目内容
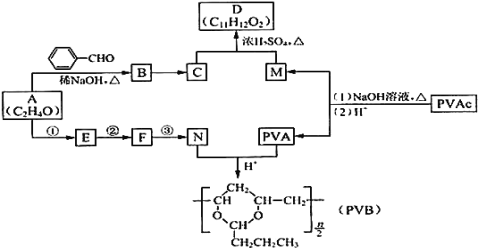
【题目】常用作风信子等香精的定香剂D以及可用作安全玻璃夹层的高分子化合物PVB的合成路线如下:
已知:Ⅰ.RCHO+R’CH2CHO![]()
![]() +H2O(R、R’表示烃基或氢)
+H2O(R、R’表示烃基或氢)
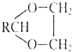
Ⅱ.醛与二元醇![]() 如:乙二醇
如:乙二醇![]() 可生成环状缩醛:RCHO+HOCH2CH2OH
可生成环状缩醛:RCHO+HOCH2CH2OH![]()
 +H2O
+H2O
⑴A的核磁共振氢谱有两种峰.A的名称是 ______
⑵下列关于B的说法正确的是 ______
a.分子式为C9H8O b.所有原子均可在同一平面上
c.最多可以与5molH2发生反应 d.可以使溴水褪色
⑶C为反式结构,由B还原得到。C的结构简式是 ______
⑷G与D含有相同的官能团,相对分子量比D小28,则G的结构有 ______ 种![]() 不包括立体异构
不包括立体异构![]()
⑸E能使Br2的CCl4溶液褪色,N由A经反应①③合成。
a.②的反应类型是 ______
b.③的化学方程式是 ______
⑹PVAc由一种单体经加聚反应得到,该单体的结构简式是 ______
⑺碱性条件下,PVAc完全水解的化学方程式是 ______
【答案】乙醛 abcd ![]() 6 加成反应 2CH3(CH2)3OH+O2
6 加成反应 2CH3(CH2)3OH+O2 ![]() 2CH3(CH2)2CHO+2H2O CH3COOCH=CH2
2CH3(CH2)2CHO+2H2O CH3COOCH=CH2 ![]() +nNaOH
+nNaOH![]()
![]() +nCH3COONa
+nCH3COONa
【解析】
根据A的分子式和A转化为B的反应条件,结合题给信息I和A的核磁共振氢谱,可以确定A为乙醛,B为![]() ;由C为反式结构,由B还原得到,可以确定C中仍具有C=C,被还原的基团应是-CHO,由此即可确定C的结构式
;由C为反式结构,由B还原得到,可以确定C中仍具有C=C,被还原的基团应是-CHO,由此即可确定C的结构式![]() ;根据D的分子式C11H12O2,可以确定其不饱和度为6,结合生成D的反应条件,可确定D为
;根据D的分子式C11H12O2,可以确定其不饱和度为6,结合生成D的反应条件,可确定D为![]() ,进而确定M为乙酸;由PVB的结构简式和题给信息II可确定其单体之一是CH3(CH2)2CHO,即N为CH3(CH2)2CHO;另一高分子化合物PVA为
,进而确定M为乙酸;由PVB的结构简式和题给信息II可确定其单体之一是CH3(CH2)2CHO,即N为CH3(CH2)2CHO;另一高分子化合物PVA为![]() ,进而推出PVAc的单体为CH3COOCH=CH2;由A和N的结构简式,结合题给信息I即可推出E为CH3CH=CHCHO,F为CH3(CH2)3OH。
,进而推出PVAc的单体为CH3COOCH=CH2;由A和N的结构简式,结合题给信息I即可推出E为CH3CH=CHCHO,F为CH3(CH2)3OH。
⑴A的分子式是C2H4O,且A的核磁共振氢谱有两种峰,因此A只能是乙醛;
⑵B为![]() ,
,
a.B的分子式为C9H8O,故a正确;
b.苯环上、碳碳双键上及碳氧双键上所有原子共面,单键可以转动,所以B的所有原子均可在同一平面上,故b正确;
c.B中有一个苯环、一个碳碳双键、一个碳氧双键,所以最多可以与5molH2发生反应,故c正确;
d.B中有碳碳双键,可以使溴水褪色,故d正确;
故选abcd;
⑶C为反式结构,说明C中含有碳碳双键.又因为C由B还原得到,B中含有醛基,因此C中含有羟基,故C的结构简式是![]() ;
;
⑷D为![]() ,G与D含有相同的官能团,即含有酯基和碳碳双键,相对分子量比D小28,即少两个碳和四个氢,则G的结构为苯环上连有-CH=CHOOCH,或-COOCH=CH2,或-OOCCH=CH2,或连有-CH=CH2、-OOCH,这样的结构有邻间对三种,所以共有6种;
,G与D含有相同的官能团,即含有酯基和碳碳双键,相对分子量比D小28,即少两个碳和四个氢,则G的结构为苯环上连有-CH=CHOOCH,或-COOCH=CH2,或-OOCCH=CH2,或连有-CH=CH2、-OOCH,这样的结构有邻间对三种,所以共有6种;
⑸根据PVB的结构简式并结合信息Ⅱ可推出N的结构简式是CH3(CH2)2CHO,又因为E能使Br2的CCl4溶液褪色,所以E是2分子乙醛在氢氧化钠溶液中并加热的条件下生成的,即E的结构简式是CH3CH=CHCHO,然后E通过氢气加成得到F,所以F的结构简式是CH3(CH2)3OH,F经过催化氧化得到N,方程式为2CH3(CH2)3OH+O2 ![]() 2CH3(CH2)2CHO+2H2O;
2CH3(CH2)2CHO+2H2O;
⑹根据上面的分析可知,PVAc的单体为CH3COOCH=CH2;
⑺PVAc为![]() ,含有酯基,能在碱性条件下水解生成
,含有酯基,能在碱性条件下水解生成![]() 和乙酸钠,反应的化学方程式为
和乙酸钠,反应的化学方程式为![]() +nNaOH
+nNaOH![]()
![]() +nCH3COONa。
+nCH3COONa。

【题目】有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 实验结论 |
(1)称取A4.5g,升温使其汽化,测其密度是相同条件下H2的45倍。 | (1)A的相对分子质量为:___。 |
(2)将此4.5g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g。 | (2)A的分子式为:____。 |
(3)另取A 4.5g,跟足量的NaHCO3粉末反应,生成1.12L CO2(标准状况),若与足量金属钠反应则生成1.12L H2(标准状况)。 | (3)写出A中含有的官能团(用结构简式表示)____。 |
(4)A的核磁共振氢谱如图: | (4)综上所述,A的结构简式为________。 |
【题目】有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 实验结论 |
(1)称取A4.5g,升温使其汽化,测其密度是相同条件下H2的45倍。 | A的相对分子质量为:___。 |
(2)将此4.5gA在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g。 | A的分子式为:___。 |
(3)另取A4.5g,跟足量的NaHCO3粉末反应,生成1.12LCO2(标准状况),若与足量金属钠反应则生成1.12LH2(标准状况)。 | 写出A中含有的官能团___、__。 |
(4)A的核磁共振氢谱如图: | 综上所述,A的结构简式为___。 |