题目内容
【题目】金属镍具有优良的物理和化学特性,是高技术产业的重要原料. 羰基法提纯镍涉及的反应为:Ni(s)+4CO(g)Ni(CO)4(g)
①当温度升高时, ![]() 减小,则△H0(填“>”或“<”).
减小,则△H0(填“>”或“<”).
②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是(填代号)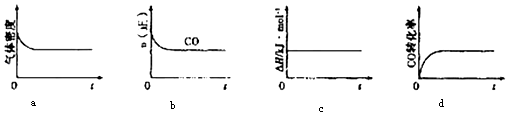
在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数(填“增大”、“不变”或“减小”),反应进行3s后测得Ni(CO)4的物质的量为0.6mol,则0﹣3s内的平均反应速率v(CO)= .
【答案】<;bd;不变;0.8mol?L﹣1?s﹣1
【解析】解:①当温度升高时, ![]() 减小,可知升高温度,平衡逆向移动,可知正反应为放热反应,所以△H<0,故答案为:<;②a.反应向正向进行,CO气体减少,生成气体Ni(CO)4密度增大,故a错误; b.反应向正向进行,CO浓度减小,速率减小,当CO正反应速率不变时说明反应掉的CO速率等于生成CO的速率,反应达到平衡状态,故b正确;
减小,可知升高温度,平衡逆向移动,可知正反应为放热反应,所以△H<0,故答案为:<;②a.反应向正向进行,CO气体减少,生成气体Ni(CO)4密度增大,故a错误; b.反应向正向进行,CO浓度减小,速率减小,当CO正反应速率不变时说明反应掉的CO速率等于生成CO的速率,反应达到平衡状态,故b正确;
c.该反应是放热反应,一定量的粗镍和CO加入一恒压密闭容器中,开始时反应正向进行,焓变发生改变,故c错误;
d.一定量的粗镍和CO加入一恒压密闭容器中,反应正向进行,CO转化率升高,达到平衡时,消耗的CO等于生成的CO,故转化率保持不变,故d正确;
平衡常数只受温度影响,所以温度不变化,平衡常数K不变;
v(Ni(CO)4)= ![]() =
= ![]() =0.2molL﹣1s﹣1 , V(CO):V(Ni(CO)4)=4:1,可知v(CO)=0.8molL﹣1s﹣1;
=0.2molL﹣1s﹣1 , V(CO):V(Ni(CO)4)=4:1,可知v(CO)=0.8molL﹣1s﹣1;
故答案为:bd;不变;0.8molL﹣1s﹣1 .
①当温度升高时, ![]() 减小,可知升高温度,平衡逆向移动;②a.反应向正向进行生成气体Ni(CO)4密度增大;
减小,可知升高温度,平衡逆向移动;②a.反应向正向进行生成气体Ni(CO)4密度增大;
b.反应向正向进行,CO浓度减小,速率减小,当CO正反应速率不变时说明反应掉的CO速率等于生成CO的速率,反应达到平衡状态;
c.该反应是放热反应,一定量的粗镍和CO加入一恒压密闭容器中,开始时反应正向进行,焓变发生改变;
d.一定量的粗镍和CO加入一恒压密闭容器中,反应正向进行,CO转化率升高,达到平衡时,消耗的CO等于生成的CO,故转化率保持不变;
平衡常数只与温度有关,温度不变化,平衡常数不变;
根据给出条件可求出用Ni(CO)4表示的3s内反应速率,然后依据反应速率之比等于方程式计量系数之比求出v(CO).

【题目】工业上产生的氮氧化物可用天然气来处理.
(1)Ⅰ.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1
N2(g)+2O2(g)=2NO2(g)△H2
H2O(l)=H2O(g)△H3
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△ H=(用△ H1、△ H2、△ H3)
(2)Ⅱ.在温度为T1℃和T2℃时,分别将0.50molCH4和1.2molNO2充入体积固定的2L密闭容器中,发生上述可逆反应,测得不同时刻的n(CH4)数据如下表:
温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
T1℃ | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2℃ | n(CH4) | 0.50 | 0.30 | 0.18 | 0.15 | 0.15 |
①分析上表中数据,下列说法正确的是
A.T1℃ 前10min,V(NO2)=0.03mol/(Lmin)
B.T1℃ 反应达化学平衡状态时,CH4的转化率为80%
C.T2℃ 反应在40min时处于平衡状态
D.T1>T2
②反应的平衡常数K(T1) K(T2),△H0,理由是 .
③T1℃时反应的平衡常数K为 .
④反应在T1℃下进行,50min时,向平衡后的容器中再通入0.10molCH4和0.40molNO2 , 在下图中画出恒温,重新达到平衡过程中n(CH4)随时间变化的曲线(只要求画出n(CH4)的变化趋势,不需要准确画出再次平衡后n(CH4) .
(3)Ⅲ.NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图.该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为 .