��Ŀ����
7��ijѧϰС��ԡ�����������ܽ��Ա�����̼���������������ʵ��̽������һ���Ʊ�̼��������
��һ�������Ʊ�������������Һ������̼�������Һ��ϲ����������������壮
��1��д�����ӷ���ʽ��Fe2++2HCO3-=FeCO3��+CO2��+H2O��
������̽��̼�����������ȶ��ԣ���������ʡ�ԣ�
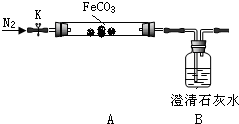
����������װҩƷ����K����ͨ��һ��ʱ�䵪����Ȼ���þƾ������A�����Ȳ����ܣ��۲�Bƿ��Һ����ǣ�������ֽ������ͨ�뵪������������ȴ��
��2����ͨ�뵪����Ŀ�����ž�װ���ڿ����������������ţ�Bƿ������˵���ֽ�����ж�����̼��
��3��ֹͣ����֮ǰ���Ƿ��A��B֮���ܣ��𣺷�������ͨ�뵪��������������ѹ�����С��
������̽��̼��������ԭ��
���������ϡ�������������һ�ֺ�ɫ��ĩ�������ȶ����ڿ����м��ȣ���Ѹ�ٱ���������������������̼�������ڿ���������������������
��4��̽��̼��������������Ӧ��Ĺ���ɷ֣�
��������롿����1 ����ɷ�����������
����2 ����ɷ���������������
����3��������������������
�����ʵ����֤����һ����ѡ�Լ���2.00mol/L��H2SO4��HCI��HNO3��KSCN��Һ��KMnO4��Һ��NaOH��Һ��H2O2��Һ��
| ʵ�鲽�� | Ԥ������ͽ��� |
���� ��1������������̼����立������ֽⷴӦ����̼������������������̼��ˮ��
��2�������β��ȶ����ױ����������������������Σ��Ӷ�����ʵ�飻
����Ԫ���غ�֪����ʹ����ʯ��ˮ����ǵ������Ƕ�����̼��
��3��ͨ�뵪��������������ѹ�����С�����Բ��������������
��4������������������������������Ļ���֤������1��ȷ��ֻҪ֤����Һ�в������������Ӽ��ɣ�����ѡ�����Ը��������Һ���飻
��5������������������ͼ�������֮��Ĺ�ϵʽ���ò�����ȷ������ɷ֣�
��� �⣺��1������������̼�������Һ��Ӧ����������李�̼��������������淋��������ӣ���̼����立�Ӧ���ɶ�����̼��ˮ����ѧ����ʽΪ��FeSO4+2NH4HCO3=FeCO3��+��NH4��2SO4+CO2��+H2O����д�����ӷ���ʽΪ��Fe2++2HCO3-=FeCO3��+CO2��+H2O��
�ʴ�Ϊ��Fe2++2HCO3-=FeCO3��+CO2��+H2O��
��2��̽��̼�������ȶ��ԣ��ų�װ���ڿ����������������+2����Ԫ�أ�B�г���ʯ��ˮ����ǣ�˵��̼�������ֽ�����ж�����̼��
�ʴ�Ϊ���ž�װ���ڿ����������������ţ��ֽ�����ж�����̼��
��3������ͨ�뵪���������С����������ѹ�����Բ��ܲ����������ز�A��B֮���ܣ�
�ʴ�Ϊ����ͨ�뵪��������������ѹ�����С��
��4��������������������������������ʼ���3Ϊ����������������������
֤������1������ɷ�����������ֻҪ֤���������������Ӽ��ɣ��������Ը��������Һ���飬��������������Ϊ��ȡ������Ӧ��Ĺ������Թ��У����������2.00mol/L��H2SO4��Һ�����ܽ⣬Ȼ�����Թ��еμ�KMnO4��Һ����KMnO4��Һ����ɫ��˵����Һ�в������������ӣ������һ������
��KMnO4��Һ��ɫ�������һ��������
�ʴ�Ϊ����������������������
| ʵ�鲽�� | Ԥ������ͽ��� |
| 1��ȡ������Ӧ��Ĺ������Թ��У����������2.00mol/L��H2SO4��Һ�����ܽ⣬ 2�����Թ��еμ�KMnO4��Һ | ��KMnO4��Һ����ɫ�������һ���� ��KMnO4��Һ��ɫ�������һ������ |
6FeCO3+O2$\frac{\underline{\;����\;}}{\;}$2Fe3O4+6CO2���徻������
6��116 232
232.2g m
��$\frac{116��6}{232}$=$\frac{23.2g}{m}$����ã�m=7.7g��7.2g��
����̼�������������и��·�Ӧ�������Ϊ������������徻������Ϊx��
4FeCO3+O2$\frac{\underline{\;����\;}}{\;}$2Fe2O3+4CO2 ���徻������
4��116 144
23.2g x
��$\frac{116��6}{144}=\frac{23.2g}{m}$����ã�x=7.2g��
�������������̼�������������и�������������������
�ʴ�Ϊ����������
���� ���⿼������ʵ�鷽����������ۣ�Ϊ��Ƶ���㣬��Ŀ�Ѷ��еȣ��漰���ӷ���ʽ����д�����ʳɷ��жϡ����Ӽ����֪ʶ�㣬ͬʱ����ѧ�������жϡ�ʵ������������������ѵ��ǣ�5���й���ɷ��жϣ�ע�����ռ��跨���������ڻ�ѧ�����е�Ӧ�ã�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���1�����������ʵ����Ʊ������в�Ҫ���ո�
| ��� | ʵ��Ŀ�� | ̼��/g | ����/g | ����/% |
| �� | Ϊ����ʵ�������� | 0.5 | 2.0 | 90.0 |
| �� | 0.5 | 2.0 | 36.0 | |
| �� | ̼��������Ӱ�� | 0.2 | 90.0 |

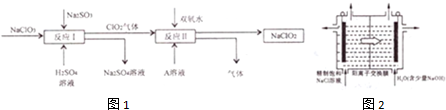
��3����С���ͼ2����0-t1ʱѹǿ����ԭ����������¼��裬������ɼ��������
����һ���������ⸯʴ���������壻
���������Ӧ����ʹ��ƿ���¶����ߣ�
��4��Ϊ��֤����һ��ijͬѧ����˼����ռ����������Ƿ���H2�ķ��������������һ��ʵ�鷽����֤����һ��
| A�� | n+11 | B�� | n-5 | C�� | n+3 | D�� | n+5 |
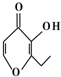 ���ӽ����̸��Ŀ��2010��10�±������׳ơ�һ���㡱���ж����ʱ���ʳ�ú�����˸��࣬�����°�����һ���㡱�ķ��ӽṹ��ͼ��ʾ������˵����ȷ���ǣ�������
���ӽ����̸��Ŀ��2010��10�±������׳ơ�һ���㡱���ж����ʱ���ʳ�ú�����˸��࣬�����°�����һ���㡱�ķ��ӽṹ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ���л�����FeCl3��Һ����ɫ | |
| B�� | 1mol���л����������3 mol H2�����ӳɷ�Ӧ | |
| C�� | ���л����ܷ���ȡ�����ӳɡ���������ȥ��Ӧ | |
| D�� | ���л����һ�ַ�����ͬ���칹���ܷ���������Ӧ |
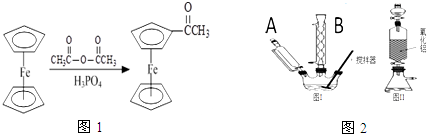
 ��������ʹ�õ�����������������������˴Ź������ף�����дһ�ּ��ɣ�
��������ʹ�õ�����������������������˴Ź������ף�����дһ�ּ��ɣ�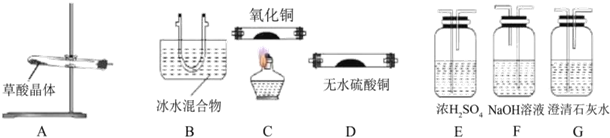
 HClO2+OH-�������ӷ���ʽ��ʾ����
HClO2+OH-�������ӷ���ʽ��ʾ����