题目内容
17.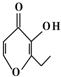 央视焦点访谈节目在2010年10月报道,俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
央视焦点访谈节目在2010年10月报道,俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )| A. | 该有机物遇FeCl3溶液显紫色 | |
| B. | 1mol该有机物最多能与3 mol H2发生加成反应 | |
| C. | 该有机物能发生取代、加成、氧化和消去反应 | |
| D. | 该有机物的一种芳香族同分异构体能发生银镜反应 |
分析 该物质中含有碳碳双键、醇羟基、羰基和醚键,具有烯烃、醇、酮、醚的性质,能发生加成反应、氧化反应、还原反应、加聚反应等,据此分析解答.
解答 解:A.该物质中不含酚羟基,所以遇氯化铁溶液不显紫色,故A错误;
B.碳碳双键和羰基能与氢气发生加成反应,1mol该有机物最多能与3 mol H2发生加成反应,故B正确;
C.该有机物含有碳碳双键、醇羟基、羰基和醚键,能发生取代、加成、氧化反应但不能发生消去反应,故C错误;
D.该有机物含有三个双键,其芳香族同分异构体含有苯环,所以苯环的支链上不可能含有醛基,导致其芳香族同分异构体不能发生银镜反应,故D错误;
故选:B.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系即可解答,侧重考查烯烃、醇的性质,易错选项是CD,注意该物质中不含苯环.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.某学习小组对“部分酸碱盐溶解性表”中碳酸亚铁的性质设计实验探究.
(一)制备碳酸亚铁.
将一定量新制备的硫酸亚铁溶液和过量的碳酸氢铵溶液混合产生大量沉淀和气体.
(1)写出离子方程式:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O.
(二)探究碳酸亚铁的热稳定性(加热仪器省略)
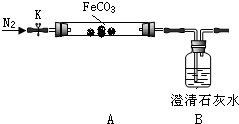
连接仪器、装药品.打开K,先通入一段时间氮气,然后,用酒精喷灯在A处加热玻璃管,观察B瓶溶液变浑浊.待固体分解完后,继续通入氮气至玻璃管冷却.
(2)先通入氮气的目的是排尽装置内空气,避免氧气干扰.B瓶现象能说明分解产物有二氧化碳.
(3)停止加热之前,是否拆开A、B之间橡胶管?答:否;理由是通入氮气,玻璃管内气压不会减小.
(三)探究碳酸亚铁还原性
【查阅资料】①氧化亚铁是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁.②碳酸亚铁在空气中灼烧生成氧化铁.
(4)探究碳酸亚铁和氧气反应后的固体成分:
【提出设想】假设1 固体成分是氧化铁;
假设2 固体成分是四氧化三铁;
假设3氧化铁和四氧化三铁.
请设计实验验证假设一(限选试剂:2.00mol/L的H2SO4、HCI、HNO3;KSCN溶液、KMnO4溶液、NaOH溶液、H2O2溶液)
(5)定量探究:取23.2g纯净固体碳酸亚铁,在空气中高温灼烧至恒重,称得固体质量净减少7.2g.通过计算确定固体成分是氧化铁.
(一)制备碳酸亚铁.
将一定量新制备的硫酸亚铁溶液和过量的碳酸氢铵溶液混合产生大量沉淀和气体.
(1)写出离子方程式:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O.
(二)探究碳酸亚铁的热稳定性(加热仪器省略)

连接仪器、装药品.打开K,先通入一段时间氮气,然后,用酒精喷灯在A处加热玻璃管,观察B瓶溶液变浑浊.待固体分解完后,继续通入氮气至玻璃管冷却.
(2)先通入氮气的目的是排尽装置内空气,避免氧气干扰.B瓶现象能说明分解产物有二氧化碳.
(3)停止加热之前,是否拆开A、B之间橡胶管?答:否;理由是通入氮气,玻璃管内气压不会减小.
(三)探究碳酸亚铁还原性
【查阅资料】①氧化亚铁是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁.②碳酸亚铁在空气中灼烧生成氧化铁.
(4)探究碳酸亚铁和氧气反应后的固体成分:
【提出设想】假设1 固体成分是氧化铁;
假设2 固体成分是四氧化三铁;
假设3氧化铁和四氧化三铁.
请设计实验验证假设一(限选试剂:2.00mol/L的H2SO4、HCI、HNO3;KSCN溶液、KMnO4溶液、NaOH溶液、H2O2溶液)
| 实验步骤 | 预期现象和结论 |
5.下列工业生产过程中,属于应用缩聚反应制取高聚物的是( )
| A. | 单体CH2═CH2制高聚物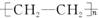 | B. | 单体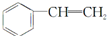 与CH2═CH-CHCH2 与CH2═CH-CHCH2制高聚物  | ||
| C. | 单体CH2═CH-CH3与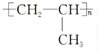 | D. | 单体 与 与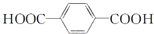 制高聚物 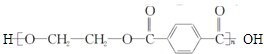 |
9.下列实验方法或叙述正确的是( )
| A. | 用分液漏斗分离水与乙酸的混合物 | |
| B. | 某溶液加氯化钡溶液有白色沉淀生成,说明原溶液中一定有SO42- | |
| C. | 过滤操作时,漏斗下部的尖嘴要紧靠烧杯的内壁 | |
| D. | 从碘水提取碘可用乙醇作萃取剂 |
6.下列关于SO2的叙述,正确的是( )
| A. | SO2与水反应生成硫酸 | |
| B. | 我国大气中SO2的主要来源是汽车排出的尾气 | |
| C. | SO2能漂白某些物质如品红溶液,说明它具有氧化性 | |
| D. | SO2既可以是含硫物质的氧化产物,又可以是含硫物质的还原产物 |
7.下列反应原理不符合工业冶炼金属实际情况的是( )
| A. | 2HgO$\frac{\underline{\;△\;}}{\;}$2Hg+O2↑ | B. | Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2 | ||
| C. | 2MgO(熔融)$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ | D. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 |




 某化学学习小组同学根据实验室现有的制取氨气的药品,设计了如图所示的实验装置(部分夹持仪器未画出),制取并探究氨气的还原性、检验反应产物.请回答下列问题:
某化学学习小组同学根据实验室现有的制取氨气的药品,设计了如图所示的实验装置(部分夹持仪器未画出),制取并探究氨气的还原性、检验反应产物.请回答下列问题: