题目内容
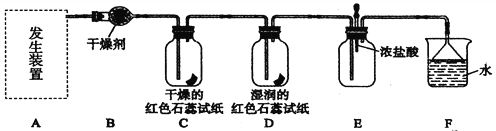
【题目】某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。
【实验探究】
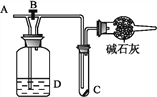
(1)实验室制取氨气应选用下图中________发生装置进行实验,反应的化学方程式为
_________________________

(2)B装置中的干燥剂可选用________(填“碱石灰”或“浓硫酸”)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是____(填“C”或“D”)。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是____________________________________________________________。
(5)F装置中倒置漏斗的作用________________________________________________。
(6)某同学用右图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有________性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(7)氨气的用途很广。如可用氨气处理二氧化氮:8NH3 + 6NO2 ==7N2 + 12H2O
该反应中氨气体现________(填“氧化性”或“还原性”)。请你列举出氨气的另一种用途_____________________________________________。
【答案】 a 2NH4Cl + Ca(OH)2 ![]() CaCl2 + 2NH3↑+2H2O 碱石灰 D 产生白烟 防止倒吸 b c 还原性 ①致冷剂②氮肥(或化肥)的原料③硝酸的原料④化工原料
CaCl2 + 2NH3↑+2H2O 碱石灰 D 产生白烟 防止倒吸 b c 还原性 ①致冷剂②氮肥(或化肥)的原料③硝酸的原料④化工原料
【解析】(1)用氯化铵和氢氧化钙在加热的条件下制备氨气,为固固加热型,选择a装置,反应的方程式为2NH4Cl + Ca(OH)2![]() CaCl2 + 2NH3↑+2H2O;(2)氨气为碱性气体,选择碱性干燥剂碱石灰干燥氨气;(3)氨气能使湿润的红色石蕊试纸变蓝,所以D中颜色发生变化;(4)氨气与挥发的HCl会生成氯化铵晶体,所以有白烟生产;(5)因为氨气极易溶于水,所以F中吸收氨气时用倒扣漏斗来防倒吸;(6)无色酚酞遇碱变红色,观察到美丽的红色喷泉,则氨气的水溶液呈碱性,氨气极易溶于水而形成压强差,导致形成喷泉;答案选bc;(7)用氨气处理二氧化氮:8NH3 + 6NO2 ==7N2 + 12H2O,该反应中,氨气中的氮元素化合价从-3价升高到0价,被氧化,表现还原性;氨气可用作①致冷剂②氮肥(或化肥)的原料③硝酸的原料④化工原料等。
CaCl2 + 2NH3↑+2H2O;(2)氨气为碱性气体,选择碱性干燥剂碱石灰干燥氨气;(3)氨气能使湿润的红色石蕊试纸变蓝,所以D中颜色发生变化;(4)氨气与挥发的HCl会生成氯化铵晶体,所以有白烟生产;(5)因为氨气极易溶于水,所以F中吸收氨气时用倒扣漏斗来防倒吸;(6)无色酚酞遇碱变红色,观察到美丽的红色喷泉,则氨气的水溶液呈碱性,氨气极易溶于水而形成压强差,导致形成喷泉;答案选bc;(7)用氨气处理二氧化氮:8NH3 + 6NO2 ==7N2 + 12H2O,该反应中,氨气中的氮元素化合价从-3价升高到0价,被氧化,表现还原性;氨气可用作①致冷剂②氮肥(或化肥)的原料③硝酸的原料④化工原料等。