题目内容
2.对于某些离子的检验及结论一定正确的是( )| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加入盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加入盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 某溶液中加入氢氧化钠溶液生成蓝色沉淀,一定有Cu2+ |
分析 A.该气体可能为二氧化碳、二氧化硫,原溶液中可能含有碳酸氢根离子、亚硫酸根离子等,不一定含有碳酸根离子;
B.加入氯化钡溶液生成的不溶于盐酸的白色沉淀可能为氯化银,原溶液中可能含有银离子;
C.能够与碳酸钠生成的溶于盐酸的白色沉淀不一定为碳酸钡,可能为碳酸钙,原溶液中可能含有钙离子;
D.加入氢氧化钠后生成的蓝色沉淀为氢氧化铜,则溶液中一定含有铜离子.
解答 解:A.将气体通入澄清石灰水中,溶液变浑浊,生成的气体可能为二氧化硫、二氧化碳,原溶液中可能存在HCO3-、SO32-等离子,不一定含有CO32-,故A错误;
B.氯化钡能与硫酸根离子或银离子结合生成不溶于水也不溶于酸的沉淀,加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液中可能含有银离子,不一定含有SO42-,故B错误;
C.碳酸钡和碳酸钙等沉淀都可溶于盐酸,原溶液中可能含有Ca2+,不一定含有Ba2+,故C错误;
D.溶液中加入氢氧化钠溶液生成蓝色沉淀,该蓝色沉淀为氢氧化铜,溶液中一定有Cu2+,故D正确;
故选D.
点评 本题考查了常见离子的性质及检验方法,题目难度中等,试题侧重于物质的检验和鉴别的考查,解答该类题目要注意排除离子的干扰的现象,注意实验的严密性.

练习册系列答案
相关题目
17. Ⅰ已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2.在温度973K和1173K情况下,K1、K2的值分别如表:
Ⅰ已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2.在温度973K和1173K情况下,K1、K2的值分别如表:
(1)通过表格中的数值可以推断:反应①是吸热(填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)?CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学
表达式:K3=$\frac{[CO]•[{H}_{2}O]}{[{H}_{2}]•[C{O}_{2}]}$.
(3)根据反应①与②可推导出K1、K2与K3之间的关系式K3=$\frac{{K}_{1}}{{K}_{2}}$.根据此关系式及表格数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应.
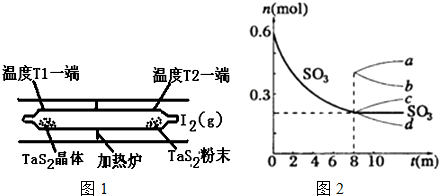
Ⅱ在一密闭容器中发生反应N2+3H2?2NH3△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
(1)处于平衡状态的时间段是ACDF(填选项字母).
A.t0~t1 B.t1~t2 C.t2~t3 D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项).
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.充入氮气
t1时刻C;t4时刻B.
(3)依据(2)中的结论,下列时间段中,氨的百分含量最低的是D(填选项字母).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
 Ⅰ已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2.在温度973K和1173K情况下,K1、K2的值分别如表:
Ⅰ已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2.在温度973K和1173K情况下,K1、K2的值分别如表:| 温度 | K1 | K2 |
| 973K | 1.47 | 2.33 |
| 1173K | 2.15 | 1.67 |
(2)现有反应③:CO2(g)+H2(g)?CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学
表达式:K3=$\frac{[CO]•[{H}_{2}O]}{[{H}_{2}]•[C{O}_{2}]}$.
(3)根据反应①与②可推导出K1、K2与K3之间的关系式K3=$\frac{{K}_{1}}{{K}_{2}}$.根据此关系式及表格数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应.
Ⅱ在一密闭容器中发生反应N2+3H2?2NH3△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
(1)处于平衡状态的时间段是ACDF(填选项字母).
A.t0~t1 B.t1~t2 C.t2~t3 D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项).
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.充入氮气
t1时刻C;t4时刻B.
(3)依据(2)中的结论,下列时间段中,氨的百分含量最低的是D(填选项字母).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
17.用下列实验装置进行相应实验,装置正确且能达到实验目的是( )
| A. | 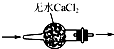 干燥SO2气体 | |
| B. |  蒸发CH3COONa溶液得醋酸钠晶体 | |
| C. |  分离有机层与水层,水层从分液漏斗下口放出 | |
| D. | 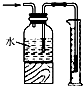 测量氯气的体积 |
11.用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 常温常压下22.4L的CO2在一定条件下与足量的镁反应,转移4NA个电子 | |
| B. | 60g SiO2中含硅氧键数目为4NA | |
| C. | 1.00mol NaCl中含有6.02×1023个NaCl分子 | |
| D. | 3.9gNa2O2中所含的阴离子数目为0.1NA |
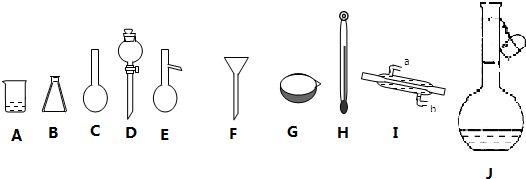
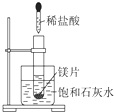 如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入一小块镁片,再用滴管滴入10mL 0.2mol/L的稀盐酸于试管中,测得生成氢气在标况的体积为11.2mL后反应停止,同时观察到盛饱和石灰水的烧杯中出现浑浊的现象.请回答下列问题:
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入一小块镁片,再用滴管滴入10mL 0.2mol/L的稀盐酸于试管中,测得生成氢气在标况的体积为11.2mL后反应停止,同时观察到盛饱和石灰水的烧杯中出现浑浊的现象.请回答下列问题: .
.