题目内容
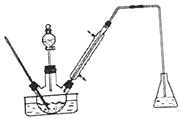
【题目】(1)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为________________。

(2)以NH3代替氢气研发燃料电池是当前科研的一个热点。使用的电解质溶液是2molL﹣1的KOH溶液,电池总反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为 ;每消耗3.4g NH3转移的电子数目为_________。
(3)用NH3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为 ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为 L。

【答案】(1)O2+2H2O+4e-=4OH-;
(2)4NH3-12e-+12OH-=2N2+12H2O;0.6NA
(3)2H2O–4e-=O2↑+4H+1.12L
【解析】
试题分析:(1)碱性环境中,该反应中负极上氢气失电子生成氢离子,电极反应式为H2+2OH--2e-═2H2O,正极上氧气得电子生成氢氧根离子,电极反应式为2H2O+O2+4e-═4OH-,故答案为: 2H2O+O2+4e-═4OH-;
(2)电池反应为:4NH3+3O2=2N2+6H2O.该电池负极是氨气失电子生成氮气,反应的电极反应式为2NH3+6OH--6e-=N2+6H2O,反应中2mol氨气反应电子转移6mol电子,每消耗3.4g NH3物质的量=![]() =0.2mol,转移的电子数为0.6NA;故答案为:2NH3+6OH--6e-=N2+6H2O,0.6NA;
=0.2mol,转移的电子数为0.6NA;故答案为:2NH3+6OH--6e-=N2+6H2O,0.6NA;
(3)用氨燃料电池电解CuSO4溶液,阳极上氢氧根离子放电,阴极上铜离子放电而析出铜,阳极上电极反应式为:4OH--4e-=O2↑+2H2O,向溶液中加入8gCuO固体后可使溶液恢复到电解前的浓度,则阳极上析出氧气的质量等于氧化铜中氧原子的质量,根据原子守恒知,氧气的体积= 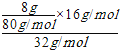 ×22.4L/mol=1.12L,故答案为:4OH--4e-=O2↑+2H2O;1.12。
×22.4L/mol=1.12L,故答案为:4OH--4e-=O2↑+2H2O;1.12。

【题目】短周期元素A、B、C、D、E的原子序数依次增大,其元素特征信息如表:
元素编号 | 元素特征信息 |
A | 最高正价和最低负价的绝对值之差为2 |
B | 和E同主族 |
C | lmo1C单质能与冷水反应,在标准状况下生成11.2LH2 |
D | 原子最外层电子数等于其周期序数 |
E | 负一价阴离子的电子层结构与Ar原子相同 |
(1) A在周期表中的位置为 。
(2)B和C形成的化合物的电子式为 。
(3)B和D简单离子的半径大小为 。
(4)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中不可行的是 (填序号)。
A.比较两种单质的颜色
B.比较两种单质与H2化合的难易程度
C.依据两元素在周期表中的位置
D.比较对应阴离子的还原性
e.比较最高价氧化物对应水化物的酸性
(5)E元素能与另外四种元素中的一种元素形成共价化合物,分子中的原子个数比为1∶3,相对分子质量为120.5,则该物质的化学式为 。