题目内容
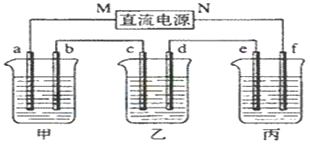
【题目】根据反应2CrO42-+2H+![]() Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是
Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是

A. a连接电源负极
B. b极反应式:2H2O-4e-=O2↑+4H+
C. c为阳离子交换膜
D. 通过2 mol电子时生成1 mol Cr2O72-
【答案】D
【解析】A.右池CrO42-转化为Cr2O72-,应增加H+浓度,b电极上OH-失电子发生氧化,促进水的电离,则b为阳极,a电极为阴极,连接电源负极,故A正确;B.b极阳极上发生氧化反应,其反应式:2H2O-4e-=O2↑+4H+,故B正确;C.与a相连的电极为阴极,阴极上氢离子失电子生成氢气,同时生成氢氧根离子,则电解后溶液中氢氧根离子浓度增大,溶液电荷不守恒,右侧溶液中Na+通过离子交换膜进入左池,则c为阳离子交换膜,故C正确;D.通过2 mol电子时右侧电极生成2molH+,促进2CrO42-+2H+![]() Cr2O72-+H2O平衡右移,根据勒夏特列原理生成Cr2O72-的物质的量小于1 mol ,故D错误;答案为D。
Cr2O72-+H2O平衡右移,根据勒夏特列原理生成Cr2O72-的物质的量小于1 mol ,故D错误;答案为D。

练习册系列答案
相关题目